Кашель является самым частым симптомом острых респираторных заболеваний (ОРЗ) у детей. Безусловно, кашель — это защитный рефлекс, направленный на восстановление проходимости дыхательных путей, однако эффективность кашля в значительной степени зависит от реологических свойств мокроты. В то же время для воспалительных заболеваний респираторного тракта характерно увеличение вязкости мокроты и снижение мукоцилиарного клиренса. Кроме того, гиперсекреция вязкой слизи, отек и бронхоспазм приводят к развитию бронхообструктивного синдрома, который ухудшает течение и прогноз болезни. Поэтому основной целью терапии острых респираторных заболеваний, сопровождающихся кашлем, является разжижение мокроты, снижение ее адгезивных свойств и облегчение эвакуации [2, 3, 4].
Несколько лет назад на российском рынке появился препарат «Проспан®» (сироп), хорошо известный в Европе. Проспан® — растительный препарат, содержащий активное вещество: сухой экстракт листьев лекарственного плюща Hedera helix.
С целью оценки клинической эффективности, переносимости и безопасности препарата растительного происхождения «Проспан®» у детей с острыми респираторными заболеваниями нами было проведено открытое сравнительное исследование. Наблюдали 263 ребенка (109 девочек и 158 мальчиков) в возрасте от 2 месяцев до 15 лет с клиническими проявлениями острой респираторной вирусной инфекции. Дети дошкольного возраста составили 84%, из них 39 (15%) — дети первого года жизни. У трети пациентов имелись в анамнезе аллергические заболевания (бронхиальная астма, атопический дерматит, аллергический ринит). 24,7% детей, включенных в исследование, были отнесены к диспансерной группе «часто болеющих детей». Хроническая ЛОР-патология имела место у 17% наблюдаемых нами детей и была представлена аденоидитом, синуситом, хроническим тонзиллитом.
Все пациенты имели схожую клиническую картину респираторной инфекции, протекающую с катаральными явлениями, признаками интоксикации, лихорадкой, приступообразным малопродуктивным кашлем. У 65 детей (24,7%) отмечались клинические признаки острого обструктивного бронхита, у 74 пациентов (28%) — острого стенозирующего ларинготрахеита (синдром крупа). Длительность заболевания на момент начала исследования у 2/3 детей составила 1–2 дня, у остальных — не более 6 суток.
Таким образом, критериями включения в исследование явилось наличие малопродуктивного кашля у детей с острыми респираторными вирусными инфекциями (ОРВИ), а критериями исключения — применение других мукоактивных препаратов менее чем за 14 дней до начала исследования, тяжелое течение бронхообструктивного синдрома с выраженными проявлениями дыхательной недостаточности и анамнестические данные о непереносимости препаратов из листьев плюща.
Все дети получали системную фармакотерапию, соответствующую тяжести основного и сопутствующих заболеваний (антибиотики, антигистамины, антипиретики и пр.). Основную группу составили 233 ребенка, которым кроме системной фармакотерапии был назначен препарат «Проспан®» в виде сиропа в рекомендуемой возрастной дозировке (детям грудного возраста — 2,5 мл × 2 раза в день, от 1 до 6 лет — 2,5 мл × 3 раза в день, с 6 до 15 лет — 5 мл × 3 раза в день). Длительность терапии составила от 7 до 15 дней. 30 больных (группа сравнения) получали системную фармакотерапию и другой фитопрепарат отхаркивающего действия (Мукалтин, микстуры с алтеем, подорожником). Распределение пациентов по группам осуществлялось методом случайной выборки. Все группы наблюдаемых детей были сравнимы по клиническому статусу.
Острая респираторная инфекция у наблюдаемых нами детей была вирусной или вирусно-бактериальной этиологии и протекала с клиническими проявлениями острого бронхита и/или ларинготрахеита. Ведущими клиническими симптомами заболевания были кашель, преимущественно малопродуктивный, симптомы острого ринита, признаки интоксикации, лихорадка. На фоне проводимой терапии у всех детей был получен хороший клинический эффект. Однако комплексная терапия ОРВИ, включающая Проспан®, способствовала более быстрой положительной динамике характера кашля: на 3 сутки от начала терапии почти у всех детей кашель стал более продуктивным, что свидетельствовало об улучшении реологических свойств мокроты. У подавляющего большинства детей (65%) частота кашля существенно уменьшилась на 5 сутки от начала терапии, через неделю кашель сохранялся только у 14% из всех наблюдаемых нами детей (рис. 1).
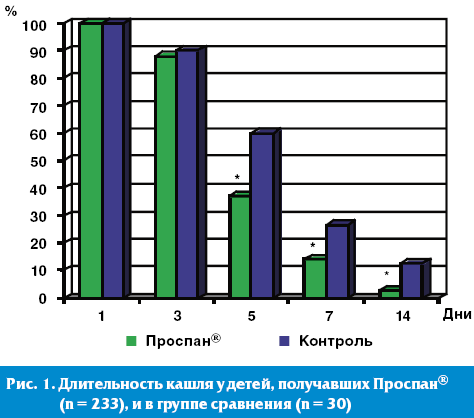
Аускультативные данные также подтвердили эффективность Проспана® как муколитика и экспекторанта, поскольку к 7 дню лечения хрипы в легких не прослушивались у большинства больных. Влажные среднепузырчатые хрипы сохранялись дольше (до двух-трех недель) только у 3 грудных детей с бронхообструкцией, причем у одного из них, кроме гипоксического поражения центральной нервной системы, был обнаружен порок развития бронхиального дерева.
Сравнительная характеристика применения Проспана® у детей с ОРВИ показала достоверно более высокую терапевтическую эффективность Проспана® по сравнению с фитомикстурами и Мукалтином.
Эффективность Проспана® в комплексной терапии острого обструктивного бронхита. Клинические признаки острого обструктивного бронхита в нашем исследовании отмечались у 65 детей (у 55 пациентов основной группы и у 10 детей группы сравнения), возраст которых составил от 5 месяцев до 13 лет, причем преобладали дети дошкольного возраста.
Представляется важным, что дети с проявлениями обструктивного бронхита на фоне ОРВИ в 28% случаев относились к диспансерной группе «часто болеющих». У 38 детей синдром бронхиальной обструкции наблюдался впервые, в остальных случаях отмечалось рецидивирующее течение бронхообструкции на фоне ОРВИ.
У 21 ребенка (30%) отмечался отягощенный семейный и личный аллергологический анамнез (атопический дерматит, пищевая и медикаментозная аллергия), однако диагноз «бронхиальная астма» у этих детей не установлен. Имели респираторные заболевания в раннем неонатальном периоде (синдром дыхательных расстройств, аспирационную пневмонию и пр.) 11 детей.
Детям с легким течением обструктивного бронхита Проспан® назначался без бронхолитической и противовоспалительной терапии. По поводу бронхообструктивного синдрома среднетяжелого и тяжелого течения дети получали бронхолитики и глюкокортикостероиды ингаляционно (Беродуал и Пульмикорт через небулайзер).
У половины пациентов, получавших Проспан®, в течение первых 3 дней отмечалась достаточно быстрая положительная динамика частоты и выраженности кашля, с полным его исчезновением к 7 дню наблюдения в 84% случаев. У пациентов из группы сравнения через неделю от начала терапии кашель сохранялся в 30% наблюдений.
На фоне комплексной терапии к 3 суткам наблюдения за счет уменьшения бронхиальной обструкции улучшилось состояние у детей основной группы: экспираторная одышка в покое исчезла, при физической нагрузке — уменьшилась (38% больных). При нагрузке до начала терапии одышка наблюдалась почти в 60% случаев в обеих группах, на третьи сутки — у 40% пациентов, частота в группах была одинакова, однако к 5 дню терапии одышка в группе сравнения была отмечена у 30% детей, в то время как в группе получавших Проспан® лишь у 4,6% детей. Через неделю одышка в покое отмечалась только у детей из группы сравнения.
Дистантные свистящие хрипы были отмечены у 1/3 детей, а к 5 дню терапии — у 4,6% пациентов основной группы и 10% — группы сравнения. К 7 дню шумного дыхания у наблюдаемых пациентов нами не отмечено. Физикальные симптомы бронхиальной обструкции до начала терапии были характерны для всех наблюдаемых детей. К 5 дню терапии симптомов бронхообструкции не было более чем у половины детей, получавших Проспан®, и у 1/3 детей из группы сравнения. К 7 дню физикальные признаки синдрома свистящего дыхания сохранялись у 30% детей группы сравнения и лишь у 13,3% пациентов, получавших Проспан®, причем у детей группы сравнения степень клинических проявлений обструкции была выше, что потребовало назначения бронхолитиков.
Необходимость в бронхолитиках при поступлении была у 13% детей основной группы и 15% — группы сравнения. На 3 сутки заболевания у части детей клинические признаки обструкции усилились, что потребовало использования бронхолитиков у 23,2% детей, получавших Проспан®, и 80% детей группы сравнения, а к 7 дню терапии — у 4,6% и 30% пациентов соответственно. Следовательно, около 80% детей с острым обструктивным бронхитом при легкой степени тяжести бронхообструкции при раннем назначении Проспана® не нуждались в бронхолитической терапии. Эти результаты представляются нам достаточно важными, т. к. в амбулаторной практике порою единственным препаратом, используемым в аналогичных ситуациях, является Эуфиллин, обладающий выраженными побочными эффектами.
Динамика суммарного индекса симптомов бронхообструкции в нашем исследовании достоверно продемонстрировала высокую эффективность раннего назначения (в первые 1–2 суток) препарата «Проспан®» у пациентов с острым обструктивным бронхитом легкого течения. К 5 дню терапии Проспаном® нами отмечено более быстрое (достоверно значимое) исчезновение симптомов бронхообструкции на фоне уменьшения клинических признаков ОРЗ по сравнению с детьми, получавшими другие отхаркивающие фитомикстуры (рис. 2).
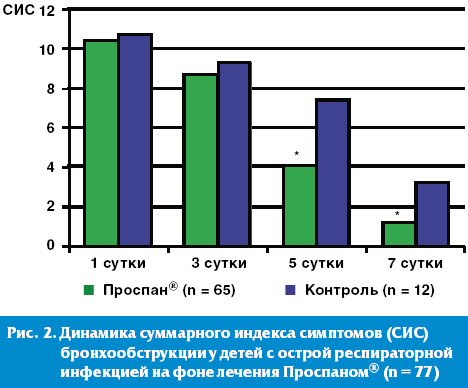
Эффективность Проспана® в комплексной терапии ОРВИ у детей с бронхиальной астмой (БА). Хорошо известно, что респираторная вирусная инфекция является триггером бронхоспазма у детей с БА. Профилактика развития приступа на фоне ОРВИ является актуальной задачей и может существенно улучшить качество жизни ребенка.
Мы наблюдали 23 детей с ОРВИ на фоне БА в периоде ремиссии основного заболевания. Все дети получали базисную терапию, соответствующую тяжести заболевания, которая при первых симптомах ОРВИ на 7 дней была увеличена в 2 раза, а в комплексную терапию были добавлены антигистамины последнего поколения.
13 детям с ОРВИ на фоне БА в комплексной терапии был назначен Проспан®, и они составили основную группу наблюдения. Группа сравнения составила 10 человек с БА и была сопоставима по тяжести и периоду заболевания с основной группой.
Бронхиальная обструкция развилась у трех (22%) детей основной группы на третьи сутки течения ОРВИ. Дыхательные расстройства имели легкую степень тяжести у двух детей (в легких с обеих сторон выслушивались рассеянные сухие хрипы, объем форсированного выдоха за 1-ю с (ОФВ1) 75–79% от нормы). Им продолжено лечение препаратом «Проспан®», на фоне чего утяжеления бронхиальной обструкции не наблюдалось. Сухой кашель через сутки стал влажным, продуктивным, к 7 дню болезни уменьшился. Хрипы в легких выслушивались 2 дня. Назначение бронхолитиков не потребовалось. У одного ребенка шести лет, страдающего бронхиальной астмой среднетяжелого течения и получающего базисную терапию ингаляционными кромонами, обструкция на фоне ОРВИ нарастала (ОФВ1 снизилась до 48% от нормы), ввиду чего усилена противовоспалительная и бронхолитическая терапия (Пульмикорт и Беродуал через небулайзер).
В группе сравнения бронхиальная обструкция клинически дебютировала у 4 детей (в 40%), по поводу чего им были назначены ингаляционные бронхолитики, а 3 пациентам — и ингаляционные глюкокортикостероиды.
Динамика суммарного индекса симптомов бронхообструкции достоверно продемонстрировала высокую эффективность раннего (в первые 1–2 суток) назначения препарата «Проспан®» у детей с ОРВИ, страдающих бронхиальной астмой (рис. 3). У этой группы пациентов назначение в комплексной терапии Проспана® в качестве отхаркивающего и секретолитического средства в первые сутки острой респираторной инфекции достоверно уменьшало и вероятность развития приступа БА.
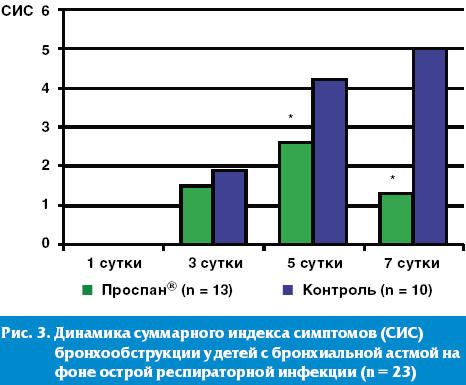
Однако, анализируя течение обструкции у детей с БА, необходимо подчеркнуть, что протективный эффект развития приступа на фоне ОРВИ у детей с БА оказывает только комплексная терапия, включающая назначение противовоспалительных препаратов (ингаляционных глюкокортикостероидов (ИГКС), фенспирида, антигистаминовых препаратов последнего поколения) и секретолитических препаратов с опосредованным бронхолитическим действием (Проспан®).
В феврале 2019 года Росздравнадзор запретил продажу в России препаратов, содержащих фенспирид, по причине возможной кардиотоксичности.
Таким образом, среди разнонаправленных эффектов экстракта из листьев плюща, а именно отхаркивающего, секретолитического и бронхоспазмолитического, наиболее уникальным и отличающим его от других препаратов от кашля (растительных или синтетических), является бронхоспазмолитическое действие. В связи с этим Проспан® можно рекомендовать и при респираторных инфекциях, сопровождающихся обструкцией. Это могут быть как острые, так и хронические состояния, протекающие с обратимым сужением дыхательных путей. Необходимо только учитывать, что бронхолитический эффект, в отличие от действия бета2-адреномиметиков, отсроченный и развивается через 24–48 часов от начала терапии, предупреждая дальнейшее прогрессирование бронхообструкции. Кроме того, в лечении обструктивных и необструктивных форм поражения бронхов всегда нужно помнить об этиологии болезни (коклюш, микоплазмоз, хламидиоз, в том числе персистирующий). Длительность респираторных симптомов и неэффективность отхаркивающей терапии часто связана с неадекватностью комплексного лечения болезни. Устранение аллергического и/или инфекционного воспаления применением антиаллергических и антибактериальных препаратов надежно купирует обострение хронического заболевания или приводит к излечению.
Эффективность Проспана® у детей первого года жизни. Известно, что в Германии Проспан® является препаратом, часто назначаемым при наличии кашля у детей раннего возраста. Это побудило нас провести анализ эффективности и безопасности препарата в этой возрастной группе.
Всего мы наблюдали 39 детей в возрасте до года с клиническими симптомами ОРВИ, из них острый ларинготрахеит отмечался у 8 пациентов, острый стенозирующий ларинготрахеит 1 степени — у 2, острый простой бронхит — у 10, острый обструктивный бронхит — у 20 детей. Треть детей находились на естественном или смешанном вскармливании. У 35% детей отмечались клинические признаки гипоксически-травматического поражения центральной нервной системы, один ребенок был с грубой задержкой психомоторного развития. Отягощенный семейный аллергологический анамнез отмечался в 5 случаях. Семь детей страдали атопическим дерматитом.
На фоне комплексной терапии, включающей Проспан®, к 3 суткам лечения кашель стал влажным у 85% больных. Длительность кашля до 6–7 дней отмечалась у 27 больных, остальные дети кашляли 2 недели и более (чаще — дети с бронхообструктивным синдромом). Они продолжали получать Проспан® до исчезновения кашля. У двух детей с синдромом бронхиальной обструкции прием Проспана® в течение пяти дней не дал облегчения откашливания мокроты и был заменен на синтетический муколитик (Лазолван) с ингаляционной доставкой в дыхательные пути через небулайзер. Все дети отлично перенесли прием препарата «Проспан®», с удовольствием его принимали, нежелательных реакций (усиления бронхореи, аллергические реакции) не наблюдалось.
Общая оценка эффективности Проспана® детям с ОРВИ, в т. ч. и при наличии бронхообструктивного синдрома, в нашем исследовании была расценена как «отличная» и «хорошая» почти у 80% больных, «удовлетворительная» у 19 пациентов (8%). Отсутствие эффекта от терапии отмечено всего у 2 из 233 детей (1%). В группе сравнения «отличный» и «хороший» эффект от проводимой терапии был отмечен у 60% пациентов, «удовлетворительный» — у 23% детей и отсутствие эффекта — у 17% больных.
Раннее назначение Проспана® было более эффективным. При использовании препарата у детей с респираторной инфекцией затянувшегося течения эффективность препарата была несколько ниже. Мы не наблюдали побочных реакций и нежелательных эффектов при назначении Проспана®, в том числе у детей с атопическими заболеваниями в анамнезе. Проспан® (сироп от кашля) обладает приятными вкусовыми качествами. Все наблюдаемые нами дети с удовольствием принимали этот лекарственный препарат.
Заключение
Таким образом, проведенное нами открытое сравнительное мультицентровое исследование показало, что Проспан® является эффективным натуральным лекарственным препаратом в терапии кашля у детей с острыми заболеваниями дыхательных путей, в том числе и у детей с обструктивным бронхитом.
Проспан® (сироп) имеет удобную расфасовку, хорошие органолептические свойства и может применяться не только в стационаре, но и в домашних условиях. Проспан® может быть рекомендован для лечения ОРВИ, протекающих с кашлем, у детей любого возраста.
По вопросам литературы обращайтесь в редакцию.
Литература
-
Белоусов Ю. Б., Омельяновский В. В. Клиническая фармакология болезней органов дыхания у детей. Руководство для врачей. Москва, 1996. 176 с.
-
Коровина Н. А. и соавт. Противокашлевые и отхаркивающие лекарственные средств в практике врача-педиатра: рациональный выбор и тактика применения. Пособие для врачей. Москва, 2002. 40 с.
-
Самсыгина Г. А., Зайцева О. В. Бронхиты у детей. Отхаркивающая и муколитическая терапия. Пособие для врачей. Москва, 1999. 36 с.
-
Противокашлевая терапия у детей. Традиционные и нетрадиционные подходы к лечению. Учебное пособие. М.: РГМУ, 2004, 96 с.
-
H.-J. Mansfeld, H. H?hre, R. Repges, U. DethlefsenMMW 140, 26–30, Vol. 3, 1998.
-
Kraft K. Tolerabiliti of dried ivy leaf extract in children Zeitschrift fur Phytoterapie. 2004, 25, 179–181.
С. И. Барденикова
О. В. Зайцева, доктор медицинских наук, профессор
Л. Н. Новожилова
Э. Э. Локшина
Т. И. Рычкова
В. А. Пастухова
Г. Б. Кузнецов
О. Б. Довгун
С. В. Зайцева
Т. Н. Празникова
И. Г. Степанова
МГМСУ, ДКБ Святого Владимира, ФГУЗ ДКБ № 38 – ЦЭП ФМБА России









