Псориатический артрит (ПсА) — это хроническое воспалительное заболевание суставов, которое развивается примерно у трети больных псориазом. Впервые описание артрита, связанного с псориазом, было дано во Франции в 1818 г. Но до 1950-х годов ПсА рассматривался как вариант ревматоидного артрита (РА). И только открытие ревматоидного фактора (РФ), анализ клинических особенностей ПсА и результатов эпидемиологических исследований, подтвердивших связь псориаза и суставного синдрома, позволили отделить ПсА от РА в самостоятельное заболевание [1].
ПсА у взрослых относится к группе серонегативных спондилоартритов. По классификации 1998 г. Дурбан ПсА у детей относится к ювенильному идиопатическому артриту.
Приблизительно с одинаковой частотой данная патология встречается среди мужчин и женщин. У детей ПсА встречается относительно редко. Его частота в структуре ювенильных артритов составляет 4–9%. Ювенильный ПсА в два раза чаще встречается у девочек. Пик заболеваемости приходится на пубертатный возраст [1].
По нашим данным из 17 пациентов с ПсА в возрасте от 3 до 17 лет 12 составляли девочки, что соответствует литературным данным. Большинство пациентов, находящихся под нашим наблюдением, заболели в возрасте до 6,5 лет, что расходится с данными литературы, остальные в период пубертата. Средний возраст начала заболевания 6,2 ± 0,5 года (минимальный 4 месяца, максимальный 15 лет). Средняя длительность заболевания составляла 6,7 ± 0,3 года.
Этиология ПсА до сих пор не выяснена. Предполагается, что наиболее существенное значение в возникновении и течении псориаза и псориатического артрита имеют генетические, иммунологические и средовые факторы.
Важность наследственности в происхождении псориатического артрита находит свое подтверждение и при анализе результатов изучения антигенов гистосовместимости (HLA) и обнаружения их связи с клиническими проявлениями заболевания. Так, при ПсА наиболее часто определяются HLA-B13, В16, В17, В27, В38, В39, DR4, DR7, HLA-B27, а по некоторым данным и В39 ассоциируются с поражением позвоночника и/или крестцово-подвздошных суставов. HLA-DR4 определяется преимущественно при полиартикулярном эрозивном процессе. Достаточно тяжелое течение артрита выявляется у носителей HLA-B17 и В38.
При иммуногенетическом обследовании, которое было проведено 8 нашим пациентам, у всех были выявлены маркеры ПсА. У четырех — НLА-В13, у двух — НLA-В16, у двух — НLА-В27). Из 17 детей 7 имели отягощенный по псориазу анамнез (родственники 1-й степени родства страдали кожным псориазом). У двух больных наследственность была отягощена по заболеванию суставов.
У детей классические проявления псориаза включают эритематозные папулы, покрытые серебристыми чешуйками, которые сливаются в бляшки различной формы. Чаще всего поражается кожа локтей, коленей, паховой области, волосистой части головы (рис. 1). Ключом к диагнозу является локализация и характер поражения суставов (например, асимметрия поражения, наличие дактилита, поражение дистальных межфаланговых суставов), которые являются основанием для тщательного осмотра паховой области, пупка и волосистой части головы с целью выявления псориатических поражений.
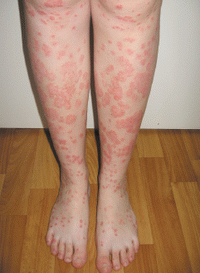
У большинства больных ПсА отсутствует четкая хронологическая зависимость между поражением кожи и суставов, хотя артрит чаще встречается у больных тяжелым псориазом. Примерно у 75% больных поражение кожи предшествует развитию артрита, у 10–15% они возникают одновременно, однако в 10–15% случаев артрит развивается раньше псориаза.
У детей в 50% случаев артрит предшествует появлению псориаза. Однако даже при наличии у ребенка симптомов этого дерматоза он обычно не столь явно выражен, как у взрослых, поэтому нередко просматривается врачами. В силу этого ювенильный ПсА часто расценивается как ювенильный РА (ЮРА), тем более что в большинстве случаев заболевание начинается с моно-, олигоартрита суставов кистей. В последующем у 40–80% детей процесс постепенно распространяется на другие суставы, хотя и в этом случае может носить асимметричный характер.
По нашим данным у 5 (29,4%) детей заболевание началось с поражения кожи (поражение суставов у этих пациентов развилось в среднем через 2,4 ± 0,3 года), а у 12 (70,6%) в дебюте наблюдался суставной синдром, причем одна больная страдала артритом без кожных изменений в течение 8 лет. Поражение кожи у этих детей присоединилось в среднем через 4,5 ± 0,8 года.
ПсА может начинаться постепенно, исподволь (первые симптомы: повышенная утомляемость, миалгии, артралгии, энтезопатии, потери массы тела). Приблизительно у трети детей в дебюте заболевания отмечаются приступообразная резкая болезненность, отек и скованность в суставах, выраженные в утренние часы.
У подавляющего большинства больных (80%) ПсА чаще проявляется артритом дистальных, проксимальных межфаланговых суставов пальцев кистей, коленных суставов, реже — пястно- и плюснефаланговых, а также плечевых суставов [1, 2, 3, 6].
По нашим данным в дебюте заболевания три пациента развернули аллергосептический синдром с лихорадкой, типичной сыпью, лимфоаденопатией, гепатолиенальным синдромом (по литературным данным вовлечение в процесс внутренних органов не характерно для ПсА). У двух в дебюте отмечалось генерализованное поражение суставов, включая шейный отдел позвоночника, по типу синдрома Стилла. У 12 — олигоартикулярный асимметричный суставной синдром, причем процесс начинался с поражения голеностопных, коленных, проксимальных межфаланговых кистей и тазобедренных суставов.
Наиболее распространено деление ПсА на пять классических форм (Moll J., Wright V., 1973):
-
асимметричный олигоартрит;
-
артрит дистальных межфаланговых суставов;
-
симметричный ревматоидноподобный артрит;
-
мутилирующий артрит;
-
псориатический спондилит.
Классификация ПсА очень условна, формы его нестабильны и могут со временем переходить одна в другую.
В 70% случаев ПсА проявляется асимметричным моно-, олигоартритом (асимметричность — характерная черта этого заболевания). ПсА свойственно также вовлечение в дебюте болезни так называемых суставов-исключений (межфалангового сустава I пальца и проксимального межфалангового — V пальца кисти). Особенностью ПсА является поражение всех суставов одного пальца кисти — аксиальный, или осевой, артрит. Нередко при этом наблюдается тендовагинит сухожилий сгибателей, что придает пораженному пальцу сосискообразный вид. Кожа над пораженными суставами, особенно пальцев кистей и стоп, нередко приобретает багровую или багрово-синюшную окраску. Вместе с тем болезненность такого сустава, в том числе и пальпаторная, обычно небольшая.
Артрит дистальных межфаланговых суставов это наиболее типичное проявление ПсА, поэтому и выделяется в отдельную форму. Но такой изолированный процесс встречается крайне редко. Намного чаще он сочетается с поражениями других суставов и псориатическим поражением ногтей. У 5% пациентов с ПсА наблюдается симметричное ревматоидоподобное поражение пястно-фаланговых и проксимальных межфаланговых суставов пальцев кистей. Иногда такая форма заболевания в дебюте создает значительные трудности в дифференциальном диагнозе с ЮРА (рис. 2).

Мутилирующий (обезображивающий) артрит является своеобразной формой ПсА и проявляется тяжелым деструктивным артритом дистальных отделов конечностей, преимущественно пальцев кистей и стоп. В результате остеолиза пальцы укорачиваются, развивается характерная деформация их («телескопический палец») или кисти («рука с лорнетом»). Возникает патологическая подвижность фаланг, приводящая к существенному нарушению функции конечности [1, 3].
Поражение позвоночника. У 40% пациентов с ПсА наблюдается вовлечение в процесс позвоночника (псориатический спондилит), причем чаще сочетающееся с артритом периферических суставов. У 5% больных наблюдается изолированное поражение осевого скелета. Изменения позвоночника при ПсА могут ничем не отличаться от изменений, свойственных болезни Бехтерева: начало — боли в поясничном отделе воспалительного характера, затем последовательное поражение грудного, шейного отделов, реберно-позвоночных суставов, формирование характерной «позы просителя». Эти больные часто являются носителями антигена гистосовместимости HLA-В27.
По нашим данным ПсА у всех пациентов протекает очень вариабельно. У 8 детей заболевание протекало с высокой лабораторной и клинической активностью, выраженным экссудативным компонентом, торпидностью к проводимой терапии. Отмечались обострения суставного и кожных изменений до 5–6 раз в год. У 9 других больных, напротив, процесс протекал легко и отмечался хороший эффект от стандартной противоревматической терапии.
В разгар заболевания через 3–4 года от начала наблюдения у 7 пациентов наблюдался симметричный ревматоидоподобный артрит, у четырех асимметричный олигоартрит, у четырех спондилоартрит с поражением периферических суставов (голеностопных, коленных, межфаланговых) и у двух пациенток мутилирующий артрит.
При ПсА отсутствуют специфические лабораторные тесты. Они лишь отражают наличие и выраженность воспалительного процесса. В активный период заболевания отмечается повышение С-реактивного белка (СРБ), серомукоида, отмечается лейкоцитоз, ускоренная СОЭ, также могут наблюдаться гемореологические нарушения [1, 3].
Рентгенологическая картина при ПсА характеризуется рядом особенностей: асимметричность рентгенологических симптомов, редкое развитие околосуставного остеопороза, наличие костной пролиферации (рис. 3, 4).
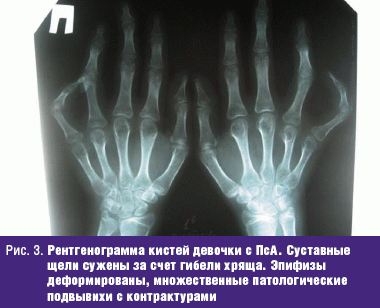
В ранних стадиях ПсА может наблюдаться околосуставной остеопороз. Но в отличие от ЮРА он чаще носит временный характер и в дальнейшем может исчезать, даже при наличии костных эрозий. Генерализованный остеопороз наблюдается при мутилирующем артрите.
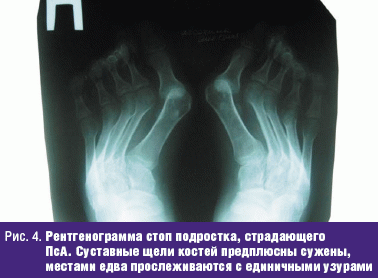
При ПсА отмечается сужение суставных щелей. Иногда деструктивный процесс в суставах пальцев кистей и стоп достаточно интенсивен, и на рентгенограммах это может выглядеть как расширение щелей суставов, что отличает ПсА от ЮРА.
Эрозии сначала появляются на краях суставных поверхностей костей, затем распространяются на центральную часть сустава. При прогрессировании деструкции костный край может заостряться и напоминать по форме заточенный карандаш. Нередко в этих случаях деформация второй сочлененной поверхности характеризуется блюдцеобразной вогнутостью, и формируется рентгенологическая картина, известная под названием «карандаш в стакане» и «чашка с блюдцем». Характерной для ПсА является деструкция межфалангового сустава I пальца стопы.
Костная пролиферация наблюдается преимущественно вокруг эрозий костей в области диафизов и эпифизов фаланг (периостит), в местах инсерций сухожилий и прикрепления связок, суставных капсул. Пролиферация кости в области эрозий возникает, видимо, как реакция на деструкцию подлежащей костной ткани. Первоначально пролифераты имеют вид небольших отростков неравномерной плотности, но в последующем они приобретают вид настоящей кости. Наиболее характерные внесуставные локализации — задние и подошвенные поверхности пяточных костей, вертелы бедренных костей, подвздошная бугристость. Длительно существующий ахиллобурсит служит причиной возникновения в пяточной кости в месте прикрепления пяточного сухожилия эрозивного процесса.
При мутилирующем артрите развивается остеолиз и резорбция суставных частей пястных, плюсневых костей, фаланг пальцев, бугорка дистальной фаланги, нередко диафизов костей предплечья. Иногда изменения развиваются довольно быстро, приводя к анкилозированию суставов уже в течение первого года болезни. В большинстве случаев анкилозы носят ярко выраженный асимметричный характер.
Иногда рентгенологические изменения позвоночника не отличаются от таковых при анкилозирующем спондилите (типичные синдесмофиты, симптом «бамбуковой палки». Характерны для псориатического спондилита так называемые парасиндесмофиты, или паравертебральные оссификаты и кальцинаты, т. е. участки оссификации (обызвествления) паравертебральных мягких тканей, остающиеся не связанными с позвонками. Для этого заболевания не характерна типичная для болезни Бехтерева «квадратизация» позвонков [1, 3].
По нашим данным в разгар заболевания у 8 пациентов (47%) отмечалась 1-я рентгенологическая стадия по Штейн–Брокеру, у 9 (53%) 3–4 рентгенологические стадии. Надо отметить, что у всех наших больных был выражен околосуставной остеопороз, что не очень характерно для ПсА. Также у 8 пациентов (47%) отмечалась 3 степень лабораторной активности, у остальных 1–2 степень. У одной больной в дебюте выявлялся положительный РФ.
Диагноз ПсА базируется на наличии ряда признаков: псориатическое поражение кожи у больного (даже незначительная по величине бляшка или наперстковидное поражение ногтевых пластинок) или кровных родственников.
При постановке диагноза псориаза существенны два симптома: признак «стеарина» (при отторжении одной чешуйки появляется белое пятно из-за сухости и ломкости покрова) и признак Аuspits (появление точечного кровотечения после соскоба чешуйки слой за слоем из-за дермического папиломатоза). Поражаются также и ногтевые пластинки. В начальной фазе появляется ряд канавок, обычно небольших, или ямок, захватывающих весь ноготь. В дальнейшем развивается фаза онихолизиса, когда ноготь выпадает из-за подлежащего гиперкератоза, частичного или тотального. Процесс начинается от края ногтя и прогрессирует по мере эволюции болезни, охватывая всю поверхность, причем одновременно ноготь становится матовым, его цвет меняется благодаря нарушениям микроциркуляции, предшествующей или сопутствующей гиперкератозу ногтевого ложа. Это часто влечет за собой осложнения в виде бактериальных или микозных вторичных инфекций.
Для диагноза имеет значение асимметричный моно-, олигоартрит, особенно с поражением пальцев кистей или стоп, аксиальный артрит, вовлечение в процесс в дебюте болезни дистальных межфаланговых суставов или суставов-исключений, асимметричный сакроилеит. Определенные трудности возникают при отсутствии у больных кожного процесса. В этих случаях следует тщательно обследовать пациента с целью поиска даже минимальных проявлений псориаза [1, 2, 3]. Для постановки диагноза используются Ванкуверовские диагностические критерии ювенильного псориатического артрита (1989).
Определенный ювенильный ПсА:
-
артрит и типичная псориатическая сыпь или
-
артрит и наличие хотя бы трех из следующих «малых» признаков:
-
изменения ногтей (синдром «наперстка», онихолизис);
-
псориаз у родственников 1-й или 2-й степени родства;
-
псориазоподобная сыпь;
-
дактилит.
Вероятный ювенильный ПсА — артрит + хотя бы два из малых признаков.
Лечение ПсА должно быть комплексным и проводиться совместно с дерматологом, в то же время нельзя надеяться на уменьшение симптомов артрита только при условии лечения кожного псориаза (например, кожные мази, положительное, ультрафиолетовое облучение (УФО), пувотерапия и т. д.). При отсутствии лечения ПсА может сильно деформировать сустав и привести к инвалидности.
Основные цели лечения при ПсА: снижение активности воспалительного процесса в суставах, позвоночнике и энтезисах — местах прикрепления сухожилий; уменьшение проявлений псориаза кожи и ногтей; замедление прогрессирования разрушения суставов; сохранение качества жизни и активности пациентов [3].
В настоящее время средств для полного излечения ПсА и псориаза не существует, но имеется множество методик, которые могут уменьшать болезненные проявления. Современные препараты позволяют управлять болезнью, полностью снимая симптомы заболевания. Однако для этого необходимо постоянное наблюдение врача и систематическое лечение.
Для лечения ПсА применяются несколько основных групп препаратов:
-
нестероидные противоспалительные препараты (НПВП). Применение традиционных НПВП (диклофенак, метиндол) предпочтительнее из-за их более активного воздействия на признаки воспаления [3];
-
глюкокортикостероиды (ГКС) применяются, главным образом, в виде периодических внутрисуставных инъекций и пульс-терапии [3];
-
базисные противоспалительные препараты (БПВП). К ним относят сульфасалазин, метотрексат, лефлуномид, циклоспорин-А. Противомалярийные (аминохинолиновые) препараты (гидроксихлорохин (Плаквенил), хлорохин (Делагил)).
Терапевтическая доза сульфасалазина составляет 30 мг/кг в сутки (доза распределяется на 2 приема). Метотрексат применяют в основном в дозе 10–15 мг/м2 в неделю в таблетках или в виде внутримышечных инъекций. Лефлуномид назначают сначала в дозе 100 мг в сутки в течение 3 дней, далее ежедневная доза составляет 20 мг (10/20 мг у детей весом до 40 кг) в сутки. Циклоспорин-А применяют в дозе 3 мг/кг. Показана эффективность этого препарата в отношении как псориаза, так и артрита. Однако на фоне терапии необходимо тщательно контролировать креатинин крови, который может повышаться, функцию печени, картину крови.
В этом случае необходимо снижение дозы препарата на 25%. Во время лечения базисными препаратами прием НПВП сохраняется. Доза НПВП может снижаться после достижения стойкого положительного результата. Препараты золота при ПсА в настоящее время не применяют из-за доказанной неэффективности и потенциальной возможности обострения псориаза. Общим правилом для всех базисных средств является строгий контроль за переносимостью препарата как со стороны врача, так и со стороны пациента (индивидуальная непереносимость). Необходимо помнить, что эффект от терапии наступает в среднем через 4–6 недель [1, 2]. При отсутствии эффекта от двух базисных средств, наличии стабильной клинической активности заболевания, острого дактилита, поражении сухожилий, изолированного псориатического спондилоартрита пациенту предлагается терапия биологическими агентами (моноклональные антитела к TNF-альфа) [3].
Инфликсимаб (Ремикейд) представляет собой химерное моноклональное антитело к фактору некроза опухоли альфа (ФНО-альфа), состоящее на 75% из человеческого белка и на 25% — из мышиного. Инфликсимаб с высокой специфичностью блокирует ФНО-альфа как циркулирующий, так и фиксированный на клеточных мембранах. Эффективность инфликсимаба (Ремикейда) при ПсА была убедительно доказана в двух рандомизированных контролируемых исследованиях (IМРАСТ и IМРАСТ 11) в целом более чем у 300 взрослых больных. Длительность наблюдения достигала 50 недель [8, 5]. C.?Antony и соавт. [9] использовали Ремикейд у 10 взрослых пациентов с тяжелым полиартикулярным псориатическим артритом (ПА). Сопутствующая терапия включала метотрексат (7 пациентов), сульфасалазин (1 пациент). У одного пациента на фоне лечения отмечено 70% улучшение клинико-лабораторных параметров с последующей длительной ремиссией в течение 5 месяцев наблюдения. У 5 пациентов к 10-й неделе также отмечена выраженная положительная динамика. При более длительном (в течение года) наблюдении этих пациентов было установлено, что у трех сохранялась ремиссия в отсутствие лечения, а у пяти ее удавалось поддерживать на фоне повторных инфузий Ремикейда в дозе 3–4 мг/кг через каждые 8–10 недель [10].
В детской практике известны лишь ограниченные случаи использования блокаторов ФНО-альфа при ПсА, что связано, конечно же, с тем, что ПсА у юных пациентов встречается гораздо реже, чем у взрослых. В нашей клинике имеется успешный опыт применения Ремикейда у детей с ПсА [5, 11]. Препарат в России зарегистрирован для детей с 6 лет.
Инфликсимаб вводится внутривенно в дозе 3 мг/кг или 5 мг/кг в сочетании с базисными препаратами. Длительность инфузии около двух часов. Вливания повторяют через 2 недели, через 6 недель, далее один раз в два месяца. Лечение проводят амбулаторно, под наблюдением врача-ревматолога. Это связано с тем, что непосредственно во время инфузии возможно падение артериального давления (АД), что требует контроля АД. Аллергические реакции возникают чаще всего во время введения первой или второй дозы препарата. Чтобы их уменьшить, снижается скорость вливания. При выраженных симптомах дополнительно пациенту назначают антигистаминные препараты и/или глюкокортикоиды. К другим побочным эффектам лечения Ремикейдом относят поражение печени, риск развития септических осложнений (например, гнойный артрит любой локализации) и Т-клеточных лимфом. Обязательным условием применения биологических препаратов является отсутствие у пациента любых признаков активной инфекции, особенно туберкулеза. С целью выявления латентного туберкулеза всем пациентам рекомендуется проводить пробу Манту и рентгенографию грудной клетки. Результат пробы Манту оценивает фтизиатр через 72 часа, он же решает вопрос о возможности применения биологических агентов [2, 12, 13, 14].
К новому поколению биологических агентов относится адалимумаб (Хумира), который может применяться как в режиме монотерапии, так и в сочетании с базисными препаратами (метотрексат). Для лечения ПсА препарат зарегистрирован в России в декабре 2006 г. В России контролируемых исследований не проводилось. Однако, по данным крупных международных исследований, у большой группы пациентов показано, что адалимумаб надежно подавляет как симптомы артрита, так и псориаза, а также задерживает рентгенологическую деструкцию суставов, улучшает качество жизни больных ПсА.?Преимуществом препарата является то, что он обладает низкой иммуногенностью, вводится пациентами подкожно в дозе 40 мг 1 раз в 2 недели, хорошо переносится больными. Наиболее распространенное нежелательное явление — постинъекционная реакция в месте введения препарата. Усиления псориаза или случаев респираторных инфекций не наблюдалось. Противопоказания для применения — те же, что и для других биологических агентов [4].
Плазмосорбция (ПС) в комплексной терапии больных псориазом является достаточно эффективным методом при различных формах болезни, обладает выраженным свойством санировать белки плазмы, что положительно влияет на восстановление белково-синтетической функции, которая значительно угнетена у больных с тяжелыми клиническими формами псориаза. Метод ПС рекомендуется применять как метод выбора при тяжелых клинических формах, особенно при торпидном течении, ПС способствует формированию длительной ремиссии и сокращает время пребывания больных в стационаре.
В период ремиссии или минимальной выраженности артрита показано санаторно-курортное лечение (Сочи, Мацеста, Пятигорск, Кемери, Кисловодск, Талги, Немиров, Краинка, Миргород) и бальнеотерапия (сероводородные, радоновые, сульфидные ванны). Бальнеотерапия используется крайне осторожно и только под наблюдение врача, в противном случае возможно обострение суставного синдрома.
Пациентам с ПсА рекомендуют вести подвижный образ жизни и ежедневно заниматься лечебной физкультурой.
Также пациентам с ПсА рекомендуется местная терапия. При лечении псориаза используют гидратирующие средства, смягчающие шелушащуюся поверхность псориатических элементов: кремы на основе ланолина с витаминными добавками, крем Унны, мазь Псориатен, которая, кроме смягчающего действия, обладает также противовоспалительным и антипролиферативным эффектом. Хороший эффект отмечается при использовании Дайвонекса, мази с антипролиферативным действием. Мази с салициловой кислотой размягчают шелушащиеся слои псориатических бляшек и ускоряют их разрешение. Также используют Антралин (Цигнолин, Дитранол). Эффективны препараты дегтя, действие которых основано на его кератопластическом, противовоспалительном и противозудном действии. Иногда эти препараты используют в сочетании с фототерапией ультрафиолетом.
Часто для лечения псориаза используют кортикостероидные мази. При псориазе предпочтение отдается кремам и мазям, содержащим, помимо стероидных гормонов, салициловую кислоту (Дипросалик, Белосалик, Лоринден А), деготь (Локакортен Тар, Лоринден Т). На участках с наиболее нежным эпидермисом и у детей рекомендуется использование негалогенизированных кортикостероидов (Адвантан).
Из нестероидных наружных лечебных средств наиболее часто при псориазе используется мазь Псоркутан, в состав которой входит кальципотриол — производное витамина D для местного применения. Широко используются в лечении псориаза витамины группы В (В1, В2, В6, В12), аскорбиновая кислота, фолиевая кислота, витамины А, Е, РР.
Подводя итог, мы можем сказать, что группа больных с ПсА очень гетерогенна и неоднородна. В последние годы появилась тенденция к более раннему началу заболевания, течение ПсА малопредсказуемо и варьируется от легких форм до тяжелых, приводящих к полной инвалидизации больного. Таким образом, по влиянию на качество жизни и функциональное состояние пациентов ПсА мало отличается от ревматоидного артрита.
Улучшить прогноз при ПсА позволяет систематическое длительное врачебное наблюдение и целенаправленная терапия с контролем лабораторных показателей и своевременной коррекцией терапии.
Литература
-
Бурдейный А.?П. Псориатический артрит. В кн. «Ревматические болезни». Под ред. Насоновой В.?А., Бунчук Н.?В. М.: Медицина. 1997, с. 314–324.
-
Бунчук Н.?В., Бадокин В.?В., Коротаева Т.?В. Псориатический артрит. В кн. «Ревматология национальное руководство». Под ред. Насонова Е.?Л., Насоновой В.?А. М.: ГЭОТАР-МЕДИА. 2008, с. 355–366
-
Taunton R.?Southwood. Psoriatic arthritis. Cassidy J.?T., Petty R.?E.?Textbook of pediatric rheumatology. Toronto, W.?B.?Saunders Company. 2002. 819 р., 345–354.
-
Бадокин В.?В. Перспективы применения ингибиторов ФНО-а при псориазе и псориатическом артрите // Клин. фармакол. тер. 2005, 14 (1), 76–79.
-
Чебышева С.?Н., Шахбазян И.?Е., Розвадовская О.?С., Мелешкина А.?В. Опыт использования инфликсимаба в лечении подростка с псориатическим артритом. В кн. «Сложный больной в практике педиатра-ревматолога». Под редакцией Н.?А.?Геппе, Т.?В.?Рябовой. М.: Медицинское информационное агентство. 2008, с. 275–281.
-
Veale D., Ritchlin С, FitzGerald О. Immunopathology of psoriasis and psoriatic arthritis // Ann. Rheum. Dis., 2005, 64 (Suppl. II), ii26–ii29.
-
McHugh N., Balakrishnan C, Jones S. Progression of peripheral joint disease in psoriatic arthritis // Rheumatology, 2003, 42, 778–783.
-
Antoni C., Krueger G., de Vlam K. et al. Infliximab improves signs and symptoms of psoriatic arthritis: results of the IMPACT 2 trial // Ann. Rheum. Dis., 2005, Feb. 24.
-
Antony C., Dechant C., Lorenz H. et al. Successful treatment of severe psoriatic arthritis with infliximab // Arthritis Rheum., 1999; 42 (Suppl.): S371.
-
Dechant C., Antoni C., Wendler J. et al. One year outcome of patients with severe psoriatic arthritis treated with infliximab // Arthritis Rheum., 2000; 43 (Suppl.): S102.
-
Чебышева С.?Н., Жолобова Е.?С., Шахбазян И.?Е., Мелешкина А.?В., Розвадовская О.?С., Геппе Н.?А. Блокаторы фактора некроза опухолей-a при псориатическом артрите у детей // рач 2010, 1, 27–28
-
Kane D., FitzGerald O. Tumour necrosis facter alpha in psoriasis and psoriatic arthritis: a clinical, genetic, and histopatholic perspective // Curr. Rheumatol. Rep., 2004, 6, 292–198.
-
Balding J., Kane D., Livingstone W. et al. Cytokine gene polymorphisms: association with psoriatic arthritis susceptibility and severity // Arthritis. Rheum., 2003, 48, 1408–1413.
-
Balding J., Kane D., Livingstone W. et al. Cytokine gene polymorphisms: association with psoriatic arthritis susceptibility and severity. Arthritis. Rheum., 2003, 48, 1408–1413.
С. Н. Чебышева, кандидат медицинских наук, доцент
Е. С. Жолобова, доктор медицинских наук, профессор
Н. А. Геппе, доктор медицинских наук
А. В. Мелешкина, кандидат медицинских наук
О. С. Розвадовская
Г. В. Михалева
ММА им. И. М. Сеченова, Москва
Контактная информация об авторах для переписки: bur@comtv.ru
Купить номер с этой статьей в pdf









