Целью нашего исследования было изучение эффективности различных методических подходов к проведению аллергенспецифической иммунотерапии (АСИТ) у больных с возможными вариантами течения атопической бронхиальной астмы (БА). Было обследовано 269 пациентов 12–23 лет, из них у 29,4% больных отмечалось легкая степень течения, у 57,2% — средняя и у 13,4% — тяжелое течение атопической БА. Базисное лечение включало использование стандартной фармакотерапии с применением ингаляционных B2-агонистов, пролонгированных теофиллинов, ингаляционных кортикостероидов и гормонов.
Обследовано 269 больных в возрасте от 12 до 23 лет, страдающих атопической БА. Средний возраст больных составил 18,8 ± 9,52 лет. Длительность заболевания к моменту обращения колебалась от 3 до 8 лет, у всех 269 больных основными причинно-значимыми аллергенами являлись бытовые и эпидермальные аллергены. Контрольная группа включала 21 здорового пациента.
В работе использованы клинико-лабораторные, функциональные, инструментальные, клинико-иммунологические и аллергологические методы обследования, которые проводились до и после лечения. Всем больным проводили prick-тесты или скарификационные кожные тесты с неинфекционными аллергенами. Для специфической диагностики и лечения аллергических заболеваний применялись стандартные серийные пыльцевые, бытовые, эпидермальные, пищевые аллергены, содержащие 10 000 PNU. Уровень специфических IgE в сыворотке крови определялся методом множественной диагностики аллергии с помощью хемилюминесцентного анализатора (MAST CLA-1).
Иммунологическое обследование включало оценку показателей иммунного статуса и проводилось в соответствии с рекомендациями Минздрава СССР (1984) иммунологической лабораторией МЗ КБР и включало: определение количества лейкоцитов в 1 мм; определение количества лимфоцитов в 1 мм (относительные и абсолютные величины); определение Т-лимфоцитов (относительные и абсолютные величины); оценка фагоцитоза (%); определение относительного и абсолютного содержания различных субпопуляций лимфоцитов (в непрямой реакции иммунофлюоресценции с моноклональными антителами). Использовалась панель МКА производства ООО «Сорбент» (Москва). Содержание Ig классов А, М, G в сыворотке крови определяли методом радиальной иммунодиффузии по Манчини, концентрацию общего IgE в сыворотке крови (МЕ/мл) — методом ИФА с помощью Anthos 2020, наборов «Dr. Fooke» (США). Уровень циркулирующих комплексов в сыворотке крови определялся по реакции с полиэтиленгликолем по Фальку.
Функциональную активность нейтрофилов оценивали микрометодом восстановления нитросинего тетразолия (НСТ-тест) по Stuart в модификации Б. С. Нагоева [8].
Исследования уровней цитокинов (ИЛ-4, ИФН-γ) осуществлялись методом твердофазного иммуноферментного анализа, с помощью наборов «CytElisa» (США), «Bender MedSystem» (США).
В зависимости от методических подходов к терапии БА все пациенты были разделены на две группы.
1-ю группу составляли 68 пациентов с атопической БА с типичным течением заболевания, которым проводилась АСИТ смесью бытовых и эпидермальных ВСЭ аллергенов по классической схеме; 2-ю группу — 201 пациент с АБА, которая протекала с клиническими проявлениями вторичной иммунной недостаточностью (ВИН) — хронические рецидивирующие воспалительные заболевания, частые ОРВИ, заболевания ЛОР-органов и др.
По степени тяжести атопическая БА в 1-й группе больных распределялась следующим образом: легкая степень течения — 30,9% (21 человек), средняя степень течения — 57,3% (39 больных), тяжелое течение — 11,8% (8 больных). Клиническая эффективность АСИТ оценивалась по 4-балльной системе в соответствии с GINA 1995. Отличный результат терапии (полная ремиссия) отмечен у 48,5 ± 7,12% (33 больных). У этих пациентов отсутствовали симптомы болезни и потребность в симпатомиметиках короткого действия, воздействие неспецифических раздражителей (холодный воздух, психоэмоциональные и физические нагрузки) не провоцировали обострения БА.
Хорошие результаты лечения (неполная ремиссия) наблюдались у 32,4 ± 8,46% (22 больных). Обострения болезни беспокоили редко, протекали легко, купировались самостоятельно.
Удовлетворительные результаты имели 19,1 ± 2,51% (13 больных). У этих пациентов сохранялись симптомы заболевания, но потребность в медикаментах значительно снизилась.
После курса АСИТ наряду с выраженным клиническим эффектом (p < 0,05) отмечалась положительная динамика функциональных показателей ФВД (табл. 1).
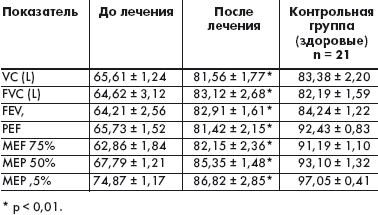 |
| Таблица 1. Средние показатели параметров ФВД до и после АСИТ (n = 68) |
Клиническая эффективность АСИТ зависела и от степени тяжести БА. При легком течении процент отличных и хороших результатов достигал 95,3%, а при среднем течении был ниже — 74,8%.
Средние величины общего lgE в группе АСИТ до лечения составили 401,2 ± 29,8 МЕ/мл, после лечения — 482,8 ± 46,9 МЕ/мл (p < 0,05).
Таким образом, наши исследования подтвердили, что при обычном, неосложненном течении атопического заболевания АСИТ является единственным патогенетическим методом терапии, позволяющим достичь стойкой клинической ремиссии и профилактического эффекта, что согласуется с мнением ряда авторов [2, 3, 4, 7, 10].
Во 2-й группе (201 пациент с атопической БА) получали комбинированную терапию АСИТ+Полиоксидоний. Все больные атопической БА этой группы имели клинические проявления ВИН. Пациенты этой группы часто (до 7–8 раз в году) страдали острыми респираторными заболеваниями, которые приводили к обострению заболевания. Течение инфекций было затяжным, торпидным к антибактериальной и противовоспалительной терапии. Из сопутствующих заболеваний со стороны ЛОР-органов гнойный гайморит и ринит диагностирован у 29,6%. Хронический бронхит выявлен у 59,5%. У 62,7% больных имелись клинические признаки нарушения микробиоценоза кишечника.
По степени тяжести атопическая БА в обследуемой группе распределялась следующим образом: легкое течение — 28,9 % (58 больных), средней степени тяжести — 57,2 % (115 больных), тяжелое течение — 13,9 % (28 больных).
Семейный аллергологический анамнез был отягощен у 63,9%.
Наличие признаков ВИН у пациентов 2-й группы служило основанием для включения в комплексную терапию иммуномодуляторов. В качестве иммуномодулятора мы использовали Полиоксидоний. Нами изучена клиническая эффективность комбинированной АСИТ при трех схемах включения Полиоксидония в комплексную терапию атопической БА.
При 1-й схеме больные получали Полиоксидоний до проведения АСИТ вместе с симптоматической фармакотерапией до достижения фармакологической ремиссии БА.
При 2-й схеме — Полиоксидоний назначали одновременно с курсом АСИТ и базисной фармакотерапией.
При 3-й схеме Полиоксидоний вводили на фоне АСИТ, начиная с разведения 10–2.
При всех трех схемах Полиоксидоний вводили внутримышечно по 6 мг, через день, всего 10 инъекций.
В ходе динамического наблюдения установлено, что наиболее высокая клиническая эффективность достигнута у больных, которым препарат вводился по 1-й и 2-й схемам. Пациенты этих групп успешно переносили инъекции АСИТ и Полиоксидония. Побочных эффектов при проведении комбинированной АСИТ не наблюдалось ни в одной из групп пациентов. Обострения острых интеркуррентных заболеваний и атопической БА на фоне лечения не возникало. Сроки проведения АСИТ в среднем составляли не более 3 мес, что соответствует срокам проведения терапии по классическому методу. У больных, получавших Полиоксидоний по 3-й схеме, т. е. начиная с разведения аллергена 10–2, АСИТ неоднократно прерывалась, из-за присоединения различных инфекций, провоцирующих обострения атопической БА. Сроки выполнения АСИТ достигали 5–6 мес.
Эффективность комбинированной АСИТ + Полиоксидоний оценивалась по динамике клинико-функциональных и иммунологических показателей. Клинические и функциональные показатели оценивались по стандартной 4-балльной системе. Отличный результат отмечался у 113 больных (56,2%), хороший — у 67 (33,4%), удовлетворительный — у 21 больного (10,4%).
Таким образом, отличные и хорошие результаты лечения составили 89,6 ± 2,51%. Отличный эффект заключался в отсутствии клинических симптомов заболевания, потребности в лекарствах и ограничения физической активности. Хороший эффект подразумевал под собой наличие обострений 1–2 раза в год, которые легко купировались бронхолитиками. Удовлетворительные результаты лечения заключались в наличии 1–2 приступов в 1–2 мес и необходимости приема β2-агонистов. Средние показатели параметров ФВД до и после терапии отражены в табл. 2.
 |
| Таблица 2. Средние показатели параметров ФВД до и после АСИТ+Полиоксидоний (n = 108) |
Также нами отмечена динамика изменений иммунологических показателей больных атопической БА в сочетании с ВИН (табл. 3).
После проведенной комплексной терапии мы имели достоверное увеличение числа CD3+ — 60,19 ± 1,12%, CD4+ — 21,0 ± 0,51%, CD8+ — 13,59 ± 0,74%, снижение уровня иммунорегуляторного индекса CD4/CD8 2,13 ± 0,04 ед и увеличение индекса ЛТИ 6,11 ± 0,11ед. Эти изменения характеризуют восстановление функциональной активности Т-лимфоцитов.
Также нами отмечено изменение показателей гуморального и фагоцитарного звеньев иммунной системы у больных с атопической БА во 2-й группе (см. табл. 3).
 |
| Таблица 3. Показатели гуморального и фагоцитарного звеньев иммунной системы у больных АБА, получивших АСИТ+Полиоксидоний (n = 108) |
После АСИТ у больных, получивших комплексную терапию, повысился уровень IgA, IgM, IgG в сыворотке крови.
Изменения выявлены и в системе нейтрофильного фагоцитоза, что характеризовалось усилением реакции НСТ-теста. Мы изучили содержание уровня цитокинов в сыворотке крови до и после проведения комбинированной АСИТ у больных атопической БА, протекающей в сочетании с ВИН.
Было установлено, что до АСИТ у больных отмечалось высокое содержание ИЛ-4 — 183,1 ± 11,0 пг/мл и низкое ИФН-γ — 34,4 ± 4,57 пг/мл, в сравнении с контрольной группой (ИЛ-4 — 19,24 ± 2,13 пг/мл, ИФН-γ — 65,0 ± 10,4 пг/мл).
После проведенной АСИТ + Полиоксидоний, отмечено достоверное снижение уровня ИЛ-4 и повышение ИФН-γ в сыворотке крови у больных атопической БА. Учитывая, что у Полиоксидония не обнаружена способность индуцировать синтез цитокинов Тh1- и Тh2-клеток: ИЛ-4 и ИФН-γ [9], изменение содержания цитокинов в сыворотке крови до и после лечения связаны с действием АСИТ.
Выводы
- При атопической БА, протекающей в сочетании с клиническими и лабораторными признаками ВИН, рекомендовано проведение АСИТ в комбинации с иммуномодуляторами.
- Показана высокая клиническая эффективность АСИТ в комбинации с иммуномодулятором Полиоксидонием у больных атопической БА, протекающей в сочетании с ВИН.
- Разработаны методические подходы и адекватные схемы включения Полиоксидония в комплексную АСИТ при атопической БА, в зависимости от вариантов клинического течения и степени тяжести БА.
- Показано нормализующее влияние комбинированной АСИТ с Полиоксидонием на показатели иммунитета и уровень цитокинов. У больных атопической БА установлена обратная корреляционная связь между уровнем IgE (r = –0,91; p < 0,01), IgG (r = –0,93, p < 0,01), эффективностью терапии (r = –0,76; p < 0,05) и длительностью ремиссии (r = –0,53; p < 0,05). Выявлена обратная зависимость между уровнем ИЛ-4 и ИФН-γ (r = –0,71; p < 0,05). Показано, что чем выше содержание ИЛ-4 в сыворотке крови у больных атопической БА после АСИТ, тем ниже клиническая эффективность терапии (r = –0,93; p < 0,01).
По вопросам литературы обращайтесь в редакцию.
М. С. Шогенова, доктор медицинских наук
Центр организации специализированной аллергологической помощи
Минздрава Кабардино-Балкарской Республики, Нальчик









