Характерной особенностью второй половины ХХ в. и настоящего времени является наличие эпидемии двух неинфекционных заболеваний — ожирения и сахарного диабета. Несмотря на значительные успехи клинической и экспериментальной диабетологии, достигнутые за последние 20 лет, распространенность и заболеваемость сахарным диабетом (СД) продолжает увеличиваться и, по данным экспертов ВОЗ, к 2010 г. в мире будет насчитываться более чем 230 млн, а к 2025 г. — 300 млн больных СД, из которых около 90% будет приходиться на больных СД 2 типа. Как указывает Z. T. Bloomgarden [1], в США в 2003 г. зарегистрировано 13,8 млн больных, страдающих СД; дополнительно к этому у 5 млн человек имеется недиагностированный СД, а у 41 млн жителей США — преддиабет. По данным Центра по контролю заболеваемости и профилактики заболеваний, в США ежегодно регистрируется 1,5 млн новых случаев сахарного диабета [2]. Увеличение распространенности сахарного диабета сопровождается повышением частоты сосудистых осложнений, которые являются, в свою очередь, причиной слепоты, хронической почечной недостаточности, ИБС и инфаркта миокарда, инсульта, нейропатии и диабетической гангрены, приводящих к ранней инвалидизации и высокой летальности.
Проведенные широкомасштабные исследования по изучению взаимосвязи степени компенсации углеводного обмена и частоты сосудистых осложнений при СД 1 типа (исследование DCCT [3]) и 2 типа (исследование UKPDS [4] и исследование Kumamoto [5]) четко продемонстрировали важность строгой компенсации СД для снижения частоты и скорости прогрессирования сосудистых осложнений.
С учетом этих данных, а также материалов других исследований целью лечения СД является достижение компенсации углеводного обмена на протяжении длительного времени, т. е. наличие показателей содержания глюкозы в плазме крови, которые практически не отличаются от таковых, наблюдаемых у здорового человека на протяжении суток.
ВОЗ и Европейская группа по политике в области диабета в 1998 г. предложили новые критерии компенсации обмена веществ у больных СД 2 типа (табл.).
Согласно рекомендациям Американской ассоциации диабета, целевые показатели гликемии должны удовлетворять следующим критериям: уровень гликозилированного гемоглобина (HbA1c) (интегрированный показатель гликемии за последние 2–3 мес) в крови больных — менее 7%, а в соответствии с руководством Международной федерации диабета — его значение должно быть ниже 6,5%.
Американская ассоциация диабета (2003) приводит для взрослых, страдающих СД, следующие биохимические показатели, свидетельствующие о компенсации диабета.
- Показатели углеводного обмена:
– HbA1c < 7,0;
– гликемия натощак (плазма) — 5,0–7,2 ммоль/л (90-130 мг/дл);
– пик постпрандиальной гликемии (плазма) < 10,0 ммоль/л (< 180 мг/дл).
- Показатели липидного обмена:
— холестерин липопротеинов низкой плотности < 2,6 ммоль/л (< 100 мг/дл);
— триглицериды < 1,7 ммоль/л (< 150 мг/дл);
— холестерин липопротеинов высокой плотности > 1,1 ммоль/л (> 40 мг/дл).
В настоящее время для проведения медикаментозной терапии больных СД 2 типа применяются препараты следующих групп:
- лекарственные средства, влияющие на снижение абсорбции углеводов в желудочно-кишечном тракте (гуарем, акарбоза, меглитол и др.);
- метформин (глиформин, формин плива, глюкофаж, сиофор и др.);
- препараты сульфонилмочевины или сульфонилмочевинные секретогены: глибенкламид, глипизид, гликлазид, гликвидон и глимепирид;
- меглитиниды, или глиниды, или секретогены инсулина производные аминокислот, обладающие коротким периодом действия: репаглинид (новонорм), натеглинид (старликс);
- тиазолидиндионы, или сенситайзеры, или глитазоны: росиглитазон (авандия), ипиоглитазон (актос).
- аналоги глюкагоноподобного пептида 1 или ингибиторы дипептидилпептидазы I и IV типа.
Если сульфонилмочевинные препараты и метформин применяются в клинической практике для лечения СД 2 типа с 60-х годов прошлого столетия, то препараты других групп — в течение последних нескольких лет. Тиазолидиндионы или глитазоны представляют собой относительно новый класс пероральных сахароснижающих препаратов. По данным H. Yki-Jarvinen [6], в 2004 г. около 20 млн больных СД получали терапию этими препаратами. Драматическая история применения первого из этой группы препаратов — троглитазона — обусловливает необходимость более тщательного рассмотрения всех аспектов их действия: эффективность и безопасность применения, влияние на различные системы и функцию различных органов организма, возможные побочные явления, встречающиеся при длительном их применении.
Наличие нескольких классов различных препаратов, применяемых для терапии СД 2 типа обусловлено тем фактом, что патогенез этого заболевания связан с инсулиновой резистентностью и недостаточностью функции β-клеток [7]. Индивидуальным сочетанием этих двух основных причин объясняется особенность течения заболевания и эффективность применяемой терапии. Клиническая практика показывает, что в одних случаях необходимо применение препаратов, первично влияющих на снижение степени выраженности инсулиновой резистентности и повышение утилизации глюкозы периферическими тканями, тогда как в других — лекарственных средств, влияющих на стимуляцию секреции эндогенного инсулина. Стимуляторы секреции инсулина — секретогены (сульфонилмочевинные препараты) применяются для лечения СД около 50 лет. Практически в течение такого же периода времени с той же целью применяется и другая группа сахароснижающих препаратов — бугианиды. Сравнительно недавно для лечения СД 2 типа были предложены новые препараты, получившие название тиазолидиндионов, или глитазонов, либо сенситайзеров инсулина (циглитазон, росиглитазон, дарглитазон, троглитазон, пиоглитазон, энглитазон), основное действие которых направлено на повышение чувствительности периферических тканей к инсулину.
Несмотря на многочисленные публикации 80–90-х годов прошлого столетия, посвященные доклиническому изучению безопасности и эффективности перечисленных соединений, в клиническую практику в дальнейшем были внедрены лишь три препарата из этой группы (троглитазон, росиглитазон и пиоглитазон).
Тиазолидиндионы усиливают действие инсулина в скелетных мышцах, жировой ткани и в печени. Механизм действия тиазолидиндионов заключается в способности этих препаратов взаимодействовать с определенным недавно идентифицированным классом ядерных рецепторов PPARγ (активируемый пролифератором пероксисом рецептор-γ), играющим основную роль в регуляции дифференцировки адипоцитов и обмена липидов. Пролифератор пероксисом, активирующий PPARs рецепторы, являющиеся подсемейством суперсемейства ядерных рецепторов, которое включает в себя 48 различных ядерных рецепторов [8], регулирующих экспрессию генов в ответ на их взаимодействие с соответствующими лигандами. Такими эндогенными лигандами для большинства рецепторов PPARs являются различные жирные кислоты, а для некоторых из них — желчные кислоты или оксистеролы [9]. В результате взаимодействия лиганда с соответствующим рецептором PPARs, последний подвергается специфическим конформационным изменениям, которые сопровождаются рекрутированием одного или нескольких белковых коактиваторов [10]. Следует подчеркнуть, что различные лиганды обладают уникальной способностью взаимодействовать с определенными коактиваторами, чем и объясняется их высоко специфический биологический ответ. Считается, что непосредственными генами-мишенями для PPARγ являются гены, кодирующие липопротеиновую липазу, белок, транспортирующий жирные кислоты, адипофилин, фосфоэнолпируваткарбоксикиназу, возможно, ген резистина и ген субстрата инсулинового рецептора 2 (СИР-2). Оставаясь центральным регулятором адипогенеза, PPARγ осуществляет дифференцировку преадипоцитов в адипоциты. Эту координирующую роль он выполняет в тесной кооперации с другими факторами транскрипции [7]. Имеется предположение, что помимо регуляции экспрессии генов, тиазолидиндионы также взаимодействуют с локусами, связывающими инсулин (определенные последовательности в субстратах инсулинового рецептора), и способствуют, таким образом, экспрессии некоторых генов, кодирующих белки, которые являются мишенью для действия инсулина, в частности транспортеры глюкозы. Модулируя инсулиновую чувствительность периферических тканей к инсулину, тиазолидиндионы участвуют также в регуляции эндокринной функции жировой ткани, изменяя секрецию соответствующих гормонов жировой ткани (фактор некроза опухолей альфа (ФНОα), ингибитор активатора плазминогена 1 типа, адипонектин, лептин и др.), что влияет на снижение скорости развития сосудистых осложнений диабета, вплоть до возможности их обратного развития.
Установлено, что механизм сахароснижающего и липидоснижающего действия тиазолидиндионов обусловлен, как отмечалось выше, их влиянием на активируемый PPARγ. PPARα, PPARγ и PPARδ относятся к семейству транскрипционных факторов, играющих центральную роль в регуляции адипогенеза и инсулиновой резистентности.
Ген PPARα экспрессируется преимущественно в печени, сердце, мышцах и сосудистой стенке. Лекарственные препараты, относящиеся к фибратам (фенофибрат, безафибрат, гемфиброзил), являются частичными или полными агонистами PPARα, активируют в печени окисление свободных жирных кислот (СЖК) (что сопровождается повышением активности карнитинпальмитоилтрансферазы 1 и 2 типа), задействованы в контроле экспрессии многих генов, участвующих в регуляции содержания и обмена липопротеинов в организме (снижают аполипопротеин С-III и увеличивают аполипопротеин А-I и II в печени), препятствуя и замедляя развитие атеросклероза, а также обладают противовоспалительными эффектами (снижение С-реактивного белка и фибриногена В в печени).
Ген PPARδ экспрессируется также во многих тканях организма, но наибольшая его экспрессия выявляется в жировых тканях, коже и мозге.
Ген PPARγ ряда млекопитающих, включая человека, локализован в 3-й хромосоме (локус 3р25). Известны три изоформы продукта указанного гена — PPARγ-1, PPARγ-2 и PPARγ-3, которые неравномерно представлены в тканях организма. Практически во всех тканях организма, включая β-клетки островков поджелудочной железы, эндотелий сосудов и макрофаги, экспрессируется PPARγ-1, тогда как PPARγ-2 — преимущественно в жировой ткани, а PPARγ-3 — в жировой ткани, макрофагах и в эпителии толстого кишечника. Установлено, что в тканях с высокой экспрессией гена PPARα (печень, сердце, скелетные мышцы), экспрессия PPARγ очень низкая или практически отсутствует.
Результаты большинства проведенных исследований подтверждают общепринятое представление о том, что PPARg опосредуют основное действие тиазолидиндионов, проявляющееся в повышении чувствительности к инсулину.
Транскрипционный фактор PPARg является основным фактором регуляции дифференцировки адипоцитов, а также способствует экспрессии белка, транспортирующего жирные кислоты, повышает экспрессию и активность ацетил-КоА-синтазы, фосфатидилинозитол-3-киназы, увеличивает экспрессию гена адипонектина, транспортера глюкозы (ГЛЮТ-4), СИР-1 и 2, подавляет экспрессию гена лептина, участвует в регуляции белков, разобщающих окислительное фосфорилирование (белки, разобщающие окислительное фосфорилирование 1, 2 и 3 типа), ингибирует экспрессию в жировой ткани ФНО-α, что сопровождается снижением инсулиновой резистентности и улучшением секреции инсулина β-клетками. Следует подчеркнуть, что в регуляцию инсулиновой резистентности оказывается вовлечен и карнитин, который также принимает участие в экспрессии PPARγ и особенно в экспрессии PPARα.
Многочисленными исследованиями установлено, что тиазолидиндионы (глитазоны) повышают чувствительность тканей к инсулину в периферических тканях как в экспериментальных условиях, так и при их применении в клинической практике. В печеночной ткани этот эффект тиазолидиндионов проявляется угнетением скорости образования глюкозы, а в других периферических тканях (жировая ткань и др.) — снижением концентрации СЖК [11]. Считается, что высокий уровень экспрессии PPARγ в жировой ткани способствует — прямо или опосредованно — повышению поглощения СЖК и их сохранению в виде жира, в жировой ткани, печени и скелетных мышцах, а возможно, и в β-клетках. В соответствии с этой точкой зрения, тиазолидиндионы, уменьшая концентрацию СЖК в циркулирующей крови больных СД 2 типа, способствуют снижению содержания триглицеридов в печени, но не в скелетных мышцах [12]. Метформин, также повышающий чувствительность периферических тканей к инсулину, оказывает этот эффект в основном в печени без изменения содержания в ней количества жира у больных СД 2 типа [13].
Однако имеются убедительные данные, свидетельствующие о том, что тиазолидиндионы, включая росиглитазон, реализуют свое влияние и через другие механизмы, не связанные со стимуляцией PPARγ. Так, B. Brunmair и соавторы [14] показали, что при исследовании in vitro на изолированных скелетных мышцах крысы шесть препаратов этой группы (троглитазон, пиоглитазон, росиглитазон и находящиеся на стадии клинических исследований ВМ 13.1258, ВМ 15.2054 и Т-174) оказывали прямое и быстрое ингибирующее воздействие на энергетический метаболизм в митохондриях, что сопровождалось быстрой — в течение 30 мин — стимуляцией высвобождения лактата под влиянием указанных средств и отсутствием эффекта от добавления к среде актиномицина D и циклогексимида, которые, как известно, являются блокаторами синтеза белка. Результаты свидетельствуют о том, что под влиянием тиазолидиндионов происходит сдвиг утилизации энергии в митохондриях от аэробного к анаэробному пути, что проявляется стимуляцией высвобождения лактата и угнетением образования СО2. При этом два других агониста PPARγ рецепторов, не относящиеся к классу глитазонов, подобным эффектом не обладали.
PPARγ является транскрипционным фактором, играющим критическую роль в регуляции дифференцировки и пролиферации адипоцитов. Кроме того, он принимает участие в экспрессии гена, который отвечает за синтез белка, транспортирующего жирные кислоты, в адипоцитах. Активация PPARγ сопровождается подавлением экспрессии гена, кодирующего лептин. Введение агонистов PPARγ животным сопровождается снижением экспрессии в жировой ткани ФНОα, который способствует инсулинорезистентности и ингибирует секрецию инсулина островками поджелудочной железы. Помимо вышеперечисленного, PPARγ регулируют экспрессию митохондриальных белков 1, 2 и 3-го типа, разобщающих окислительное фосфорилирование, и вызывают также экспрессию сигнального белка cCbl, принимающего участие в действии инсулина. Кроме того, один из препаратов этой группы, пиоглитазон, обладает дополнительными свойствами, а именно — вызывает усиление экспрессии гена аР2, продукт которого участвует в механизмах сахароснижающего действия препаратов этой группы.
Таким образом, становится понятно, что действие глитазонов, приводящее к образованию популяции более чувствительных к инсулину жировых клеток [15, 16], связано с их влиянием на экспрессию генов в адипоцитах и активизацию дифференцировки преадипоцитов в адипоциты. В недавно опубликованной работе van Harmelen и соавторов [17] четко показано влияние различных тиазолидиндионов (троглитазона, пиоглитазона и росиглитазона) на процессы дифференцировки адипоцитов в жировой ткани сальника и подкожного депо. В культуре жировой ткани с минимальной степенью дифференцировки адипоцитов через 16 дней инкубации количество м-РНК лептина и его секреция повышались в 2–6 раз в подкожно-жировой ткани, по сравнению с жировой тканью сальника. Наряду с этим показатели липолиза, стимулированного норадреналином, были в 2 раза выше в жировой ткани сальника по сравнению с подкожно-жировой тканью.
В США тиазолидиндионы в качестве антидиабетических средств применялись с 1997 г. и были представлены тремя препаратами этой группы — троглитазоном (с 1997 г.), росиглитазоном и пиоглитазоном (с мая и июля 1999 г., соответственно).
Троглитазон — первый препарат этой группы — был синтезирован в 1983 г. В его химическую структуру входят группы, характерные как для тиазолидиндиона, так и витамина Е. С 1997 г. препарат применялся для лечения больных СД 2 типа. Уже через 2 года более 1 млн больных в США, Японии и Великобритании принимали этот препарат.
На фоне широкого использования троглитазона для лечения больных, появились данные о его побочных воздействиях, в числе которых нарушение функции печени, вплоть до развития острой печеночной недостаточности. К марту 1999 г. были опубликованы 43 наблюдения, относящихся к острой печеночной недостаточности. При этом у 9 из указанных больных была проведена трансплантация печени и у 28 пациентов осложнение закончилось летальным исходом. Средний возраст больных составил 63 года (43–91 год), при этом 70% пациентов составляли лица женского пола. Длительность терапии троглитазоном — от 4 до 236 дней (в среднем — 116 дней). У 69% больных суточная доза троглитазона составила 400 мг, у 20% — 200 мг и у 11% — 600 мг. На момент постановки диагноза у 89% пациентов имелась желтуха, которая в 62% случаев служила первым симптомом. Период от появления желтухи до развития энцефалопатии в среднем составлял 19 дней (от 0 до 70 дней). Посмертные гистологические исследования, проведенные у больных, показали наличие гепатоцеллюлярного некроза. По данным R. S. Sherwin [17], за 3 года клинического применения троглитазона в США было зарегистрировано 90 случаев недостаточности функции печени у больных, получавших указанный препарат. Из них 63 случая закончились летальным исходом. Расчеты показали, что риск летальности от недостаточности печени у больных, получавших терапию троглитазоном, составляет 1 на 100 000. В связи с выраженной гепатотоксичностью в марте 2000 г., по решению Комиссии по контролю за лекарствами и продуктам питания (FDA), троглитазон был изъят из списка лекарственных веществ, рекомендованных для широкого применения в клинической практике в США.
Высокая гепатотоксичность, выявленная у троглитазона, не является характерной для всех препаратов этой группы. Влияние пиоглитазона и роcиглитазона на активность печеночных ферментов сравнима с этим показателем у больных, получавших плацебо во время проведения первой фазы клинических исследований.
Изучение воздействия тиазолидиндионов на состояние углеводного обмена проводилось многими исследователями. Так, T. P. Ciaraldi и соавторы [19] установили, что у больных СД 2 типа, у которых отсутствовал эффект от применения глибенкламида, на фоне приема троглитазона отмечалось увеличение массы тела на 5 кг, в подкожно-жировом слое области живота увеличивался объем адипоцитов и повышалось содержание лептина в сыворотке крови, тогда как масса тела пациентов, получавших терапию метформином, оставалась стабильной, уменьшался объем (до 84% от контрольного уровня) адипоцитов, а содержание лептина в сыворотке крови оставалось без изменений. Инсулинстимулированное распределение глюкозы в организме под влиянием метформина увеличивалось на 20%, а под влиянием троглитазона — на 44% — по сравнению с исходными данными. При этом у больных, получавших терапию метформином, в адипоцитах содержание белков ГЛЮТ-4 не изменялось, тогда как после терапии троглитазоном количество белка ГЛЮТ-4 увеличивалось в 2 раза. Кроме того, под влиянием троглитазона возрастало на 170% инсулинстимулированное фосфорилирование протеинкиназы В, а под влиянием метформина фосфорилирование указанной киназы оставалось без изменений. Результаты исследований показывают, что тиазолидиндионы регулируют транспорт глюкозы в адипоциты, повышая экспрессию ГЛЮТ-4, и активируют сигнальные инсулиновые пути, что проявляется повышенным распространением глюкозы во все ткани организма.
Очень близкие результаты были получены K. A. Virtanen и соавторами [20], которые изучали влияние росиглитазона (4 мг 2 раза в день) и метформина (1 г 2 раза в день) у больных СД 2 типа. Уровень поглощения глюкозы в организме определялся посредством позитронно-эмиссионной томографии с использованием дидеоксиглюкозы, а количество жировых депо — с помощью магнитно-резонансной томографии. Под влиянием монотерапии росиглитазоном улучшалось на 44% инсулинстимулированное поглощение глюкозы тканями организма. Масса тела у больных, получавших росиглитазон, не изменялась, тогда как под влиянием терапии метформином она уменьшалась на 2 кг. На фоне терапии росиглитазоном (авандия) поглощение глюкозы висцеральным жировом депо увеличивалось на 29%, тогда как под влиянием метформина — на 17%. Однако под влиянием росиглитазона отмечалось четкое увеличение поглощения глюкозы жировыми депо бедренной области. Авторы исследования считают, что терапия метформином способствует улучшению гликемического контроля без увеличения периферической чувствительности к инсулину, тогда как росиглитазон повышает инсулиновую чувствительность в подкожной жировой ткани различной локализации, чем и объясняется улучшение чувствительности к инсулину в организме. Этот положительный эффект на повышение чувствительности периферических тканей к инсулину является опосредованным через влияние инсулина на снижение уровня СЖК. Параллельно этому под влиянием росиглитазона улучшается чувствительность к инсулину как в мышцах, так и в целом организме.
Опыт клинического применения тиазолидиндионов показывает, что одним из нежелательных или побочных влияний указанных препаратов является повышение и без того высокой массы тела пациентов. Однако, как показали специально проведенные исследования, увеличение массы тела при этом происходит за счет подкожного, а не висцерального депо жировой ткани, количество которого имеет высоко статистически достоверное влияние на степень выраженности инсулиновой резистентности и повышенный риск развития сердечно-сосудистых осложнений.
Доказано, что умеренное увеличение массы тела, наблюдаемое у больных СД 2 типа на фоне терапии глитазонами, происходит за счет подкожного жирового депо. Так, D. E. Kelley и соавторы [21] установили, что на фоне приема росиглитазона при умеренном увеличении массы тела отмечалось уменьшение на 10% количества висцерального депо жира, что снижает риск развития сердечно-сосудистых заболеваний.
Особый интерес представляет исследование P. C. Davidson и соавторов [22], в ходе которого изучалось влияние пиоглитазона (45 мг) и росиглитазона (8 мг) на течение диабета у больных, ранее получавших лечение троглитазоном. Если на приеме троглитазоном у больных СД 2 типа содержание гликозилированного гемоглобина в крови снизилось с 8,1 до 7,5%, то под влиянием пиоглитазона у этих больных отмечалось дальнейшее его снижение — до 7,1% — с максимальным наступлением эффекта через 6 мес.
В группе больных, получавших росиглитазон, уровень гликозилированного гемоглобина не изменился (7,9% после лечения троглитозоном и 7,9% после терапии росиглитазоном). Снижение содержания триглицеридов и повышение холестерина липопротеинов высокой плотности в сыворотке крови было более выраженным у больных, получавших пиоглитазон, по сравнению с росиглитазоном. Что касается общего холестерина и холестерина липопротеинов низкой плотности, то у пациентов, получавших пиоглитазон, отмечалось уменьшение этих показателей, тогда как у больных, проходящих курс лечения росиглитазоном, указанные показатели повысились. Однако у пациентов, получавших пиоглитазон, за время лечения выявлена прибавка в весе (в среднем на 2,5 кг), тогда как у больных, получавших росиглитазон, масса тела снизилась в среднем на 400 г.
Таким образом, тиазолидиндионы (сенситайзеры или глитазоны) являются высокоаффинными агонистами PPARy, которые повышают чувствительность тканей к инсулину, что сопровождается снижением уровня глюкозы, липидов и инсулина в сыворотке крови как в экспериментах на животных, так и у больных СД 2 типа.
Следует указать, что дополнительно к тиазолидиндионам разработан новый класс агонистов к PPARs-рецепторам — глитазары, которые активируют в основном PPARa-рецепторы и в значительно меньшей степени — PPARg. К глитазарам относится тезаглитазар и мураглитазар (Mura), которые на различных стадиях клинических испытаний характеризуются эффективным воздействием на течение липидного и углеводного обмена у больных СД 2 типа.
В совместном заявлении Американской диабетической ассоциации и Европейской ассоциации по изучению сахарного диабета [23] указано, что лечение сахарного диабета 2 типа рекомендуется начинать с назначения метформина одновременно с изменением образа жизни.
Если лечение оказывается безуспешным, на втором этапе дополнительно рекомендуется прием инсулина (снижение гликозилированного гемоглобина на 1,5–2,5%), препаратов сульфонилмочевины (снижение гликозилированного гемоглобина на 1,5%), тиазолидиндионов (снижение гликозилированного гемоглобина на 0,5–1,4%), ингибиторов a-глюкозидаз (снижение на 0,5–0,8%), экзенатида (снижение гликозилированного гемоглобина на 0,5–1%), глинидов (снижение гликозилированного гемоглобина на 1–1,5%), прамлинтида применяется в США (снижение гликозилированного гемоглобина на 0,5–1%).
Недавно опубликованные результаты [24] многоцентрового, рандомизированного, двойного слепого исследования ADOPT (Diabetes Outcome Progression Trial) по применению монотерапии росиглитазоном, метформином или глибенкламидом 4360 больных с вновь выявленным СД 2 типа, показали, что росиглитазон уменьшает риск потери эффективности монотерапии на 32% по сравнению с метформином (p < 0,001) и на 63% по сравнению с глибуридом (глибенкламидом) (p < 0,001) в течение 5 лет. Вероятно, это связано с тем, что росиглитазон статистически значимо (p < 0,001) улучшает чувствительность к инсулину по сравнению с метформином и глибенкламидом) и уменьшает степень нарушения функции β-клеток (p = 0,02 по сравнению с метформином и p < 0,001 по сравнению с глибенкламидом) островкового аппарата поджелудочной железы.
В том случае, если на фоне изменения образа жизни, применения метформина и перечисленных дополнительных сахароснижающих препаратов не удается достичь желаемого результата (уровень гликозилированного гемоглобина в крови менее 7%), то следует проводить интенсивную инсулиновую терапию, на время которой отменяются секретогены (препараты сульфонилмочевины или глиниды). Интенсивную инсулиновую терапию можно комбинировать с приемом метформина или глитазонов. При этом следует иметь в виду, что применение глитазонов у некоторых больных может сочетаться с задержкой в организме жидкости. В тех случаях, когда течение диабета сопровождается гипергликемией выше 10% в сочетании с кетонурией, полидипсией, полиурией и снижением массы тела, терапией выбора является лечение инсулином. Основной целью лечения СД 2 типа является достижение строгой компенсации углеводного обмена, что является основанием для снижения риска развития сердечно-сосудистых осложнений диабета.
Литература
- Bloomgarden Z. T. Developments in diabetes and insulin resistance// Diabetes Care. 2006; Vol. 29: 161–167.
- Center for Disease Control and Prevention. National Diabetes Surveillance System. (Acccessed November 14, 2006, at http://www.cdc.gov/diabetes/statistics.).
- The DCCT Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus// N Engl J Med. 1993; Vol. 329: 977–986.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33)// Lancet. 1998; Vol. 352: 837–853.
- Ohkubo Y., Kishikawa H., Araki E. et al. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with NIDDM: a randomized prospective 6-year study// Diabetes Res Clin Pract. 1995; Vol. 28: 103–117.
- Yki-Jarvinen H. Drug therapy: thiazolidinediones// N. Engl J Med. 2004; Vol. 351: 1106–1118.
- Балаболкин М. И., Клебанова Е. М., Креминская В. М. Лечение сахарного диабета и его осложнений (руководство для врачей). М.: Медицина, 2005. С. 511.
- Chawla A., Repa J. J., Evans R. M., Mangelsdorf D. J. Nuclear receptors and lipid physiology: opening the X-files// Science. 2001; Vol. 294: 1866–1870.
- Berger J., Moller D. E. The mechanisms of action of PPARs// Annu Rev Med. 2002; Vol. 53: 409–435.
- Wilson T. M., Lambert M. H., Kliewer S. A. Peroxisome proliferator-activated receptor gamma and metabolic disease// Annu Rev Biochem. 2001; Vol. 70: 341–367.
- Miyazaki Y., Glass L., Triplitt C. et al. Effect of rosiglitazone on glucose and nonesterified fatty acid metabolism in type 2 diabetes patients// Diabetologia. 2001; Vol. 44: 2210–2219.
- Bajaj M., Suraamornkul S., Pratipanawatr T. et al. Pioglitazone reduces hepatic fat content and augments splanchnic glucose uptake in patients with type 2 diabetes// Diabetes. 2003; Vol. 52: 1364–1370.
- Tiikkainen M., Hakkinen A. M., Korshninnikova E. et al. Effects of rosiglitazone and metformin on liver fat content, hepatic insulin resistance, insulin clearance and gene expression in adipose tissue in patients with type 2 diabetes// Diabetes. 2004; Vol. 53: 2169–2176.
- Brunmair B., Gras F., Neschen S. et al. Direct thiazolidinedione action on isolated rat skeletal muscle fuel handling is independent of peroxisome proliferator-activated receptor-(-mediated changes in gene expression// Diabetes. 2001; Vol. 50: 2309–2315.
- Walczak R., Tontonoz P. PPARadigmas and PPARadoxes. Expanding roles of PPAR( in the control of lipid metabolism// J. Lipid Res. 2002; Vol. 43: 177–186.
- Arner P., Free fatty acids-do they play a central role in type 2 diabetes?// Diabetes Obes Metab. 2001; Vol. 3: 11–19.
- Van Harmelen V., Dicker A., Ryden M. et al. Increased lipolysis and decreased leptin production by human omental as compared with subcutaneous preadipocytes// Diabetes. 2002; Vol. 51: 2029–2036.
- Sherwin R. S. Clinical experience with thiazolidinediones// Management strategies refined: the emerging role of thiazolidinediones in type 2 diabetes// Symposium of 36-th meeting of EASD. Jerusalem, 17-th Sep. 2000.
- Ciaraldi T. P., Kong A. P. S., Chu N. V. et al. Regulation of glucose transport and insulin signaling by troglitazone or metformin in adipose tissue of type 2 diabetic subjects// Diabetes. 2002; Vol. 51: 30–36.
- Virtanen K. A., Hallsten K., Parkkola R. et al. Differential effects of rosiglitazone and metformin on adipose tissue glucose uptake in type 2 diabetes// Diabetes. 2003; Vol. 52: 283–290.
- Kelley D. E., McKolanis T. M., Kelley C. A. Comparative effects of rosiglitazone and metformin on fatty liver and visceral adiposity in type 2 diabetes mellitus// Diabetes. 2002; Vol.51; Suppl. 2: A35.
- Davidson P. C., Sabbah H., Steed R. T. et al. Pioglitazone versus rosiglitazone therapy in randomized follow-up in patients previously treated with troglitazone// Diabetes. 2001; Vol. 50; Suppl 2: A109 (437-P).
- Nathan D. M., Buse J. B., Davidson M. B. et al. Management of hyperglycaemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy// Diabetologia. 2006; Vol. 49: 1711–1721.
- Kahn S. E., Haffner S. M., Heise M. A. et al. Glycemic durability of rosiglitazone, metformin, or glyburide monotherapy // N Engl J Med. 2006; Vol. 355: 2427–2443.
М. И. Балаболкин, доктор медицинских наук, профессор
Е. М. Клебанова, кандидат медицинских наук
В. М. Креминская, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
Приложения
-
- Роль тиазолидиндионов в компенсации углеводного обмена при СД 2 типа и в предупреждении сосудистых осложнений диабета - Таблица.
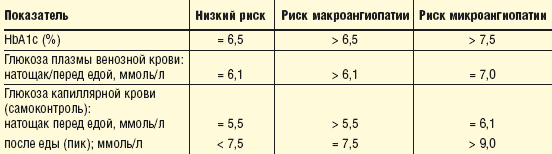
Критерии компенсации СД 2 типа









