Вторичные иммунные тромбоцитопении, возникающие на фоне ряда лимфопролиферативных опухолей и гемобластозов, вызывают наибольшие сложности в плане фармакотерапии [1]. Многофакторный патогенез, развитие тромбоцитопении и геморрагического синдрома уже на фоне или после использования иммунодепрессантов создают предпосылки для развития множества побочных эффектов, а прогрессирование геморрагического синдрома при достигнутой ремиссии основного заболевания не только негативно отражается на качестве жизни пациента, но и представляет непосредственную угрозу его жизни [2, 3]. Это предполагает нестандартный подход к лечению таких больных, с применением в составе комплексной терапии нетоксичных современных иммунодепрессантов, отличающихся избирательностью воздействия.
Больная Л., 53 года, в течение 3 лет наблюдается с диагнозом множественная миелома, тип IgG, II стадии, диффузно-очаговая форма. Проводилась полихимиотерапия с использованием схем VCP (винкристин, циклофосфан, преднизолон), VMCP (с включением ломустина), в результате в течение 2 лет была достигнута ремиссия миеломной болезни, что подтверждалось данными миелограммы (доля плазматических клеток составляла 7%), исчезновением парапротеина, нормализацией СОЭ. В дальнейшем курсы полихимиотерапии не проводились, однако присоединилась аутоиммунная тромбоцитопения тяжелого течения, характеризующаяся ежемесячными рецидивами с яркими клиническими (образование множественных экхимозов по всей поверхности тела, десневые кровотечения) и лабораторными проявлениями (число тромбоцитов 5–7 х 109/л). Аутоиммунный характер тромбоцитопении подтверждался данными мегакариоцитограммы (наличие мегакариоцитоза в пунктате), а также клинико-анамнестическими показателями (цикличность проявлений геморрагического синдрома, отсутствие в лекарственном анамнезе цитостатиков на протяжении 6 мес до начала клинических проявлений геморрагического синдрома). Нарастающий геморрагический синдром послужил в дальнейшем причиной неоднократных госпитализаций в стационар. Фармакотерапия с использованием вводимого внутривенно в дозе 60 мг преднизолона и одновременным применением метипреда — по 40 мг в сутки — способствовала наступлению кратковременных ремиссий (число тромбоцитов не более 30–50 х 109/л) с последующим обострением, наступавшим через 3 нед, и развитием тех же клинических и лабораторных изменений.
В иммунном статусе регистрировались признаки аутоиммунного синдрома с гиперактивацией CD4-лимфоцитов, гипериммуноглобулинемией классов М и G, активацией системы комплемента и накоплением высокого уровня патогенных циркулирующих иммунных комплексов. Отмечалось также повышенное содержание γ-глобулина крови, выраженное снижение соотношения альбумины/глобулины.
Известно, что в развитии иммунной тромбоцитопении наибольшее значение имеют антитела против гликопротеина IIb/IIIa преимущественно класса G, повреждающее воздействие которых и приводит к прогрессирующему снижению числа тромбоцитов [4]. Однако, несмотря на то что продукция IgG обеспечивается гиперстимулированными В-лимфоцитами, первичная роль в патогенезе заболевания отводится дисфункции Т-лимфоцитов, нарушению соотношения Th-1/Th-2 и, соответственно, цитокиновому дисбалансу при гиперпродукции интерлейкина-4. В результате происходит не только повреждение зрелых тромбоцитов, но и нарушение мегакариоцитопоэза [5].
Тимодепрессин — иммунодепрессант нового поколения, представляет собой синтетический дипептид последовательности γ-D-Glu-D-Trp (C16H20N3O5), который способен подавлять патологическую продукцию Th-2 интерлейкина-4, являющегося одним из значимых факторов отклонения иммунного ответа по гуморальному типу, и тормозить развитие аутоиммунных реакций [6].
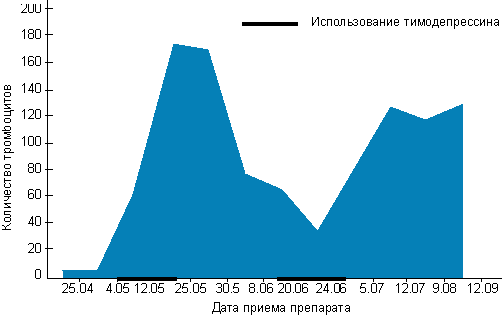
Фармакотерапию с использованием тимодепрессина (0,1% раствор, внутримышечно, 2 курса по 5 инъекций с 5-дневным интервалом [7]) в этой ситуации сочетали с назначением преднизолона в более низких, чем ранее (без комбинации с тимодепрессином), дозах (30 мг, внутривенно) на протяжении всего периода лечения. В результате отмечались восстановление числа тромбоцитов, нормализация содержания иммуноглобулинов сыворотки крови, снижение уровня патогенных циркулирующих иммунных комплексов. Однако через 3 нед после окончания лечения вновь наблюдался рецидив заболевания, характеризующийся резким снижением числа тромбоцитов и клиническими проявлениями геморрагического синдрома. Проводимая повторно фармакотерапия включала более длительные, 7-дневные, курсы тимодепрессина, преднизолон использовался в прежнем режиме. Проведенное лечение в целом способствовало достижению субнормальных показателей числа тромбоцитов (до 126 х 109/л) и устранению клинических проявлений геморрагического синдрома на протяжении последующих 2,5 мес. Таким образом, после 4-го курса тимодепрессина в сочетании с преднизолоном была достигнута стойкая ремиссия заболевания (рис.). Отмечались хорошая переносимость проводимой фармакотерапии и отсутствие значимых нежелательных эффектов (регистрировался лишь кратковременный субфебрилитет).
На основании вышеизложенного можно сделать следующие выводы.
- Тимодепрессин является эффективным и безопасным средством комплексной фармакотерапии вторичной иммунной тромбоцитопении, что позволяет в ходе комбинированной фармакотерапии использовать более низкие дозы глюкокортикостероидов и свести к минимуму риск их нежелательных эффектов.
- Для достижения стабильной ремиссии вторичной иммунной тромбоцитопении у пациентов с миеломной болезнью целесообразно проводить не менее 4 курсов терапии с использованием тимодепрессина в сочетании с глюкокортикостероидами, продолжительность лечения должна составлять 5-7 дней; в дальнейшем показаны курсы поддерживающей фармакотерапии тимодепрессином.
Литература
- Kumar M., Vik T. A., Johnson C. S., Southwood M. E. et al. Treatment, outcome, and cost of care in children with idiopathic thrombocytopenic purpura//Am. J. Hematol. 2005; 78: 181-187.
- Beardsley D. S. Pathophysiology of immune thrombocytopenic purpura// Blood. Rev. 2002; 16: 13-14.
- Huber M. R., Kumar S., Tefferi A. Treatment advances in adult immune thrombocytopenic purpura//Ann Hematol. 2003; 82: 723-737.
- Sandler S. G. Review: immune thrombocytopenic purpura: an update for immunohematologists// Immunohematology. 2004; 20: 112-117.
- Zhou B., Zhap H., Yang R. C., Han Z. C. Multi-dysfunctional pathophysiology in ITP. Crit. Rev. Oncol// Hematol. 2005; 54(2): 107-116.
- Семенец Т. Н., Семина О. В., Виноградова Ю. Е., Дейгин В. И. и др. Использование синтетических иммуномодулирующих пептидов для восстановления кроветворения у мышей после цитостатика цитозин-арабинозида (Ара-Ц)//Иммунология. 2000. № 6. С. 20-22.
- Виноградова Ю. Е., Замулаева И. А., Павлов В. В., Селиванова Е. И. и др. Применение тимодепрессина для лечения аутоиммунных цитопений//Тер. архив. 2002. № 8. С. 64-67.
А. М. Бударин, кандидат медицинских наук
И. М. Пелипас
А. Ю. Одокиенко, кандидат медицинских наук
Ю. В. Редькин, доктор медицинских наук, профессор
Омская областная клиническая больница, Омск
Приложения
-
- Препарат тимодепрессин в лечении миеломной болезни - Рисунок. Динамика числа тромбоцитов на фоне иммунодепрессивной фармакотерапии