В повседневной практике в стационаре клиницисту приходится сталкиваться с двумя группами инфекционных болезней. К первой из них относятся внебольничные инфекции — инфекционные процессы, возникшие вне стационара и по поводу которых пациент поступил в стационар. Ко второй группе — госпитальные (внутрибольничные, нозокомиальные) инфекции, развившиеся у пациента в стационаре.
Практически важные различия между двумя указанными группами инфекционных болезней касаются их этиологической структуры и антибиотикорезистентности возбудителей. Для внебольничных инфекций характерен ограниченный и достаточно стабильный состав наиболее вероятных возбудителей, зависящий от локализации инфекционного процесса. Спектр возбудителей госпитальных инфекций, как правило, несколько менее предсказуем. Возбудители внебольничных инфекций, в сравнении с возбудителями госпитальных, характеризуются также существенно меньшим уровнем антибиотикорезистентности. Указанные различия важны для выбора рациональной эмпирической терапии инфекций в стационаре.
В стационарах в условиях тесного контакта между отдельными пациентами, а также между больными и персоналом появляется возможность обмена штаммами микроорганизмов. Параллельно на фоне интенсивного применения антибиотиков происходит селекция антибиотикорезистентных штаммов.
В результате в лечебных учреждениях складывается микроэкологическая ситуация, характеризующаяся доминированием определенных штаммов микроорганизмов и преобладанием среди них антибиотикорезистентных штаммов. Доминирующие в лечебном учреждении штаммы называют госпитальными. Четких критериев, позволяющих признать тот или иной штамм госпитальным, не существует. Антибиотикорезистентность является важным, но необязательным признаком.
При попадании в стационар происходит неизбежный контакт пациента с госпитальными штаммами бактерий. При этом, по мере удлинения сроков пребывания в лечебном учреждении, возрастает вероятность замены собственной микрофлоры пациента госпитальной, а соответственно и развития инфекций, вызванных госпитальной микрофлорой. Точно установить срок, в течение которого происходит колонизация нестерильных локусов пациента госпитальной микрофлорой, достаточно сложно, так как это определяется многими факторами (возраст, нахождение в палатах интенсивной терапии, тяжесть сопутствующей патологии, антибиотикотерапия или применение антибиотиков с профилактической целью). Соответственно так же сложно установить временной интервал — когда возникающую инфекцию следует считать госпитальной. В большинстве случаев инфекция считается таковой при проявлении клинической симптоматики через 48 и более часов от момента госпитализации пациента.
Оценить частоту госпитальных инфекций в нашей стране сложно из-за отсутствия официальной регистрации данных заболеваний. По данным международных многоцентровых исследований, средняя частота госпитальных инфекций в лечебных учреждениях составляет 5–10% [1–3], а в отделениях реанимации и интенсивной терапии (ОРИТ) достигает 25–49% [4–6]. В значительной части исследований, посвященных этиологии госпитальных инфекций, отражена ситуация в тех стационарах, в которых выполнялись данные работы. Поэтому их результаты могут быть экстраполированы на другие учреждения лишь с большой долей условности. Даже многоцентровые исследования не могут считаться исчерпывающими, хотя и являются наиболее репрезентативными.
Наиболее полноценно изучена структура и этиология инфекций в ОРИТ. По данным многоцентрового исследования, проведенного в один день в 1417 ОРИТ 17 стран Европы и охватившего более 10 тыс. пациентов, находившихся на лечении, у 44,8% пациентов были выявлены те или иные инфекции, причем частота ОРИТ-ассоциированных инфекций составила 20,6% [6]. Наиболее часто в ОРИТ регистрировались пневмония (46,9%), инфекции нижних дыхательных путей (17,8%) и мочевыводящих путей (ИМВП) (17,6%), ангиогенные инфекции (12%). В этиологической структуре инфекций доминировали грамотрицательные бактерии семейства Enterobacteriaceae (34,4%), Staphylococcus aureus (30,1%), Pseudomonas aeruginosa (28,7%), коагулазонегативные стафилококки (КНС) (19,1%), грибы (17,1%). Многие этиологически значимые микроорганизмы характеризовались устойчивостью к традиционным антибиотикам, в частности встречаемость метициллинрезистентных стафилококков составила 60%, в 46% случаев P. aeruginosa была устойчива к гентамицину [7].
Сходные результаты, касающиеся этиологической структуры инфекций, были получены в другом исследовании [4], в ходе которого также было установлено, что большинство пациентов, находящихся в ОРИТ (72,9%), получали антибиотики с лечебной или профилактической целью. Наиболее часто назначались аминогликозиды (37,2%), карбапенемы (31,4%), гликопептиды (23,3%), цефалоспорины (18,0%). Спектр применяемых препаратов косвенно подтверждает высокий уровень антибиотикорезистентности в ОРИТ.
В рамках системы контроля за госпитальными инфекциями в США (NNIS) проводится постоянный мониторинг госпитальных инфекций и антибиотикорезистентности. В 1992–1997 гг. было выявлено превалирование в ОРИТ инфекций мочевыводящих путей (31%), пневмонии (27%), первичных ангиогенных инфекций (19%), причем 87% первичных ангиогенных инфекций были связаны с центральными венозными катетерами, 86% пневмоний — с искусственной вентиляцией легких (ИВЛ) и 95% мочевых инфекций — с мочевыми катетерами [5]. Ведущими возбудителями пневмонии, связанной с ИВЛ (нозокомиальная пневмония при ИВЛ — НПивл), были Enterobacteriaceae (64%), P. aeruginosa (21%), S. aureus (20%); среди возбудителей ангиогенных инфекций были КНС (36%), энтерококки (16%), S. aureus (13%), грибы (12%). При мочевых инфекциях доминировали грибы и Enterobacteriaceae.
Таким образом, в этиологической структуре наиболее частых форм госпитальных инфекций наибольшее значение имеют пять групп микроорганизмов, на долю которых приходится до 90% всех случаев заболеваний: Staphylococcus aureus; КНС, среди которых наибольшее значение имеют S. epidermidis и S. saprophyticus; энтерококки, прежде всего E. faecalis и E. faecium; Еnterobacteriaceae, среди которых доминируют E. coli, Klebsiella spp., Enterobacter spp., Proteus spp., Serratia spp.; группа неферментирующих бактерий, прежде всего P. aeruginosa и в меньшей степени Acinetobacter spp.
На основании первичной локализации очага инфекции можно судить о предполагаемой этиологии заболевания, что, безусловно, служит надежным ориентиром в выборе эмпирического режима антибактериальной терапии (табл. 1).
Сложности лечения госпитальных инфекций зависят от следующих факторов:
- тяжести состояния больного, обусловленной основным заболеванием;
- частого выделения из раны или брюшной полости двух и более микроорганизмов;
- возросшей в последние годы резистентности микроорганизмов к традиционным антибактериальным препаратам, прежде всего пенициллинам, цефалоспоринам, аминогликозидам, фторхинолонам.
Кроме того, необоснованное, часто бессистемное применение антибиотиков ведет к быстрой селекции и распространению в рамках стационара устойчивых штаммов микроорганизмов.
Проведение рациональной антибактериальной терапии госпитальных инфекций невозможно без современных знаний об этиологической структуре инфекционных заболеваний и антибиотикорезистентности их возбудителей. На практике это означает необходимость выявления микробиологическими методами этиологического агента инфекции и оценки его антибиотикочувствительности. Только после этого речь может идти о выборе оптимального антибактериального препарата.
Однако в практической медицине ситуация не так проста, и даже самые современные микробиологические методики часто не в состоянии дать клиницисту быстрый ответ или даже вообще уточнить возбудителя заболевания. В этом случае на помощь приходят знания о наиболее вероятных этиологических агентах конкретных нозологических форм госпитальных инфекций (табл. 1), спектре природной активности антибиотиков и уровне приобретенной резистентности к ним в данном регионе и конкретном стационаре. Последнее представляется наиболее важным при планировании антибактериальной терапии госпитальных инфекций в стационаре, где отмечается наиболее высокий уровень приобретенной резистентности, а недостаточная оснащенность микробиологических лабораторий и низкий уровень стандартизации исследований по оценке антибиотикочувствительности не позволяют сформировать реальное представление об эпидемиологической ситуации в медицинском учреждении и разработать взвешенные рекомендации по лечению.
Из наиболее распространенных в стационарах нашей страны механизмов антибиотикорезистентности следует выделить следующие, имеющие наибольшее практическое значение.
- Стафилококки, устойчивые к метициллину (оксациллину). Метициллинрезистентные стафилококки проявляют устойчивость ко всем β-лактамным антибиотикам (пенициллинам, цефалоспоринам, карбапенемам), включая ингибиторзащищенные, а также ассоциированную устойчивость ко многим другим группам препаратов, включая аминогликозиды, макролиды, линкозамиды, фторхинолоны. Эти микроорганизмы во всех случаях сохраняют чувствительность только к ванкомицину и линезолиду, бoльшая часть из них также чувствительны к рифампицину, фузидину, ко-тримоксазолу.
- Энтерококки, устойчивые к ванкомицину (VRE). С высокой частотой встречаются в ОРИТ США, данные по нашей стране отсутствуют, однако сообщения о выделении VRE имеются. VRE сохраняют чувствительность к линезолиду, в некоторых случаях — к ампициллину.
- Микроорганизмы семейства Enterobacteriaceae (прежде всего Klebsiella spp. и E. coli), продуцирующие β-лактамазы расширенного спектра и устойчивые к цефалоспоринам I, II, III поколений. Наиболее надежны в данном случае карбапенемы, в некоторых случаях активность сохраняют цефепим и цефоперазон/сульбактам. Среди других механизмов устойчивости энтеробактерий следует отметить гиперпродукцию некоторыми представителями (прежде всего Enterobacter spp., Serratia spp., Citrobacter freundii) хромосомных β-лактамаз класса С, которые также эффективно гидролизуют цефалоспорины III поколения и, кроме того, не чувствительны к действию ингибиторов β-лактамаз (клавулановая кислота, сульбактам, тазобактам). Против этих микроорганизмов активность сохраняют цефепим и карбапенемы.
- P. aeruginosa, устойчивая ко многим антибиотикам вплоть до панрезистентных штаммов. Предсказать фенотип устойчивости P. aeruginosa в каждом конкретном случае сложно, поэтому особое значение приобретают локальные данные по антибиотикорезистентности. В последние годы увеличилась распространенность штаммов P. aeruginosa, проявляющих устойчивость к карбапенемам, цефалоспоринам. Из наиболее активных антипсевдомонадных антибиотиков следует выделить цефтазидим, цефепим, меропенем, амикацин.
Учитывая указанные сложности лечения госпитальных инфекций (тяжесть состояния пациентов, часто полимикробный характер инфекции, возможность выделения при нозокомиальных инфекциях возбудителей со множественной устойчивостью к антибактериальным средствам), необходимо сформулировать следующие принципы рационального применения антибиотиков в стационаре.
- Антибактериальную терапию следует начинать неотложно при регистрации инфекции до получения результатов бактериологического исследования.
- Выбор стартового эмпирического режима терапии должен осуществляться с учетом вероятного спектра возбудителей (табл. 1) и их возможной резистентности (данные локального мониторинга антибиотикорезистентности).
- Первоначальная оценка эффективности терапии проводится в течение 48–72 ч после начала лечения по уменьшению выраженности лихорадки и интоксикации. Если в эти сроки не наблюдается положительного эффекта, то режим терапии следует скорректировать.
- Профилактическое применение антибиотиков в послеоперационном периоде (при отсутствии клинических признаков инфекции) следует признать нерациональным и нежелательным.
- Введение антибиотиков следует осуществлять в соответствии с официальными инструкциями. Основные пути введения — внутривенный, внутримышечный, пероральный. Другие способы (интраартериальный, эндолимфатический, внутрибрюшной, эндотрахеальный и др.) не имеют доказанных преимуществ по сравнению с традиционными.
Выбор антибактериального препарата может осуществляться на основании установленной этиологии заболевания и уточненной чувствительности возбудителя к антибиотикам — такую терапию определяют как этиотропную. В других ситуациях, когда возбудитель не определен, препарат назначается эмпирически. В последнем случае выбор антибиотика основывается на вероятном спектре микроорганизмов, вызывающих инфекцию определенной локализации, и знании основных тенденций антибиотикорезистентности наиболее вероятных возбудителей. Понятно, что в клинической практике до уточнения этиологии заболевания эмпирический подход используется наиболее часто.
При тяжелых инфекциях принципиально важно назначение уже на первом этапе лечения адекватного режима антибактериальной терапии, что подразумевает применение эмпирической терапии с максимально полным охватом всех потенциальных возбудителей инфекции данной локализации. Этот принцип стартовой эмпирической терапии, проводимой в полном объеме, особенно актуален при лечении таких инфекций, как НПивл, перитонит, сепсис, так как установлено, что в случае неадекватной стартовой терапии достоверно увеличивается риск летального исхода [8–10]. По нашим данным [11], в случае неадекватного выбора стартовой эмпирической терапии НПивл риск летального исхода увеличивается в 3 раза.
Адекватная эмпирическая антибактериальная терапия должна отвечать следующим требованиям.
- Выбранный режим терапии охватывает всех потенциальных возбудителей инфекции.
- При выборе антибактериального препарата учитывается риск селекции полирезистентных штаммов возбудителей.
- Режим антибактериальной терапии не должен способствовать селекции в отделении резистентных штаммов бактерий.
Рекомендации по эмпирическому назначению антибактериальных препаратов для лечения госпитальных инфекций во всех случаях будут иметь очень условный характер, так как они не учитывают локальные данные по уровню антибиотикорезистентности в каждом конкретном медицинском учреждении. Поэтому в представленных ниже рекомендациях лишь оговаривается перечень антибиотиков, потенциально наиболее эффективных при конкретных инфекциях с учетом глобальных тенденций и состояния антибиотикорезистентности в стране, причем в связи с этим препараты перечисляются в алфавитном порядке. В лечебных программах приведенные режимы антибактериальной терапии разделены на две группы — оптимальные средства и альтернативные средства.
Под оптимальными средствами подразумеваются режимы антибактериальной терапии, применение которых, по мнению автора и с позиций доказательной медицины, позволяет с наибольшей долей вероятности достичь клинического эффекта. При этом также учитывался принцип разумной достаточности, т. е. по возможности в качестве средств выбора рекомендовались антибиотики с наиболее узким спектром антимикробной активности.
При составлении представленных рекомендаций авторы также принимали во внимание ряд документов, опубликованных в последние годы [12–15].
Антибактериальная терапия проводится до достижения стойкой положительной динамики состояния пациента и исчезновения основных симптомов инфекции. В связи с отсутствием патогномоничных признаков бактериальной инфекции абсолютные критерии прекращения антибактериальной терапии установить сложно. Обычно вопрос о прекращении антибиотикотерапии решается индивидуально, на основании комплексной оценки динамики состояния пациента. В общем виде критерии достаточности антибактериальной терапии могут быть представлены следующим образом:
- нормализация температуры тела (максимальная дневная температура < 37°С);
- положительная динамика основных симптомов инфекции;
- отсутствие признаков системной воспалительной реакции;
- отрицательная гемокультура.
Сохранение только одного признака бактериальной инфекции (лихорадка или лейкоцитоз) не является абсолютным показанием для продолжения антибактериальной терапии. Имеются исследования, показывающие, что во время нахождения пациентов в ОРИТ на ИВЛ достижение нормальной температуры, исчезновение лейкоцитоза и стерилизация трахеи маловероятны даже на фоне адекватной антибактериальной терапии [16]. Изолированная субфебрильная лихорадка (максимальная дневная температура в пределах 37,9°С) без ознобов и изменений в периферической крови может быть проявлением постинфекционной астении или небактериального воспаления после оперативного вмешательства и не требует продолжения антибактериальной терапии, так же как и сохранение умеренного лейкоцитоза (9–12 х 109/л) при отсутствии сдвига влево и других признаков бактериальной инфекции.
Обычные сроки антибактериальной терапии госпитальных инфекций различной локализации составляют от 5 до 10 дней. Более длительная антибиотикотерапия не желательна из-за развития возможных осложнений лечения, риска селекции резистентных штаммов и развития суперинфекции. При отсутствии стойкого клинико-лабораторного ответа на адекватную антибактериальную терапию в течение 5–7 дней необходимо проведение дополнительного обследования (УЗИ, КТ и др.) для выявления осложнений или очага инфекции другой локализации.
В определенных клинических ситуациях требуются более длительные режимы антибактериальной терапии. Обычно такой подход рекомендуется для инфекций, локализующихся в органах и тканях, в которых терапевтические концентрации антибиотиков труднодостижимы и, следовательно, имеется более высокий риск персистирования возбудителей и рецидивов инфекции. Это относится прежде всего к остеомиелиту, инфекционному эндокардиту, вторичному гнойному менингиту. Кроме того, при инфекциях, вызванных S. aureus, обычно также рекомендуют более длительные курсы антибактериальной терапии — 2–3 нед.
Представленные схемы антибактериальной терапии действенны в отношении наиболее характерных и часто встречающихся в медицинской практике госпитальных инфекций. Вместе с тем некоторые сложные клинические ситуации не рассматриваются в рамках данной статьи, так как с трудом поддаются стандартизации. В таких случаях вопрос о тактике лечения следует решать совместно со специалистом по антимикробной химиотерапии или клиническим фармакологом.
Литература
- Haley R. W., Culver D. H., White J.W. et al. The nationwide nosocomial infection rate: a new need for vital statistics. Am J Epidemiol 1985; 121: 159–167.
- Intensive Care Antimicrobial Resistance Epidemiology (ICARE) Surveillance Report, data summary from January 1996 through December 1997: a report from the National Nosocomial Infections Surveillance (NNIS) System. Am J Infect Control 1999; 27: 279–284.
- Centers for Disease Control and Prevention. Detailed ICU surveillance component: national nosocomial infection surveillance scheme 1-80. Atlanta, GA: Centers for Disease Control and Prevention, 1997.
- Esen S., Leblebicioglu H. Prevalence of nosocomial infections at intensive care units in Turkey: a multicentre 1-day point prevalence study. Scand J Infect Dis 2004; 36(2): 144–148.
- Richards M. J., Edwards J. R., Culver D. H., Gaynes R. P. Nosocomial infections in medical intensive care units in the United States. National Nosocomial Infections Surveillance System. Crit Care Med 1999; 27(5): 887–892.
- Vincent J. L., Bihari D. J., Suter P. M. et al. The prevalence of nosocomial infection in intensive care units in Europe: results of the European Prevalence of Infection in Intensive Care (EPIC) Study. EPIC International Advisory Committee. JAMA 1995; 274: 639–644.
- Vincent J. L. Microbial resistance: lessons from EPIC study. European prevalence of infection. Intensive Care Med 2000; 26: 1: 3–8.
- Kollef M. H., Sherman G., Ward S., Fraser V. J. Inadequate antimicrobial treatment of infections: a risk factor for hospital mortality among critically ill patients. Chest 1999; 115(2): 462–474.
- Iregui M., Ward S., Sherman G., Fraser V. J., Kollef M. H. Clinical importance of delays in the initiation of appropriate antibiotic treatment for ventilator-associated pneumonia. Chest 2002;122(1):262–8.
- Dupont H., Mentec H., Sollet J. P., Bleichner G. Impact of appropriateness of initial antibiotic therapy on the outcome of ventilator-associated pneumonia. Intensive Care Med 2001;27(2):355–62.
- Yakovlev S., Gelfand B., Protsenko D. Ventilator-associated pneumonia in patients with truma: risk factors concerning mortality [abstract P1603]. 13th European Congress of Clinical Microbiology and Infectious Diseases, Glasgow, May 10–13, 2003. Clin Microbiol Infect 2003; 9 (6).
- Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. Am J Respir Crit Care Med 2005; 171: 388–416.
- Solomkin J. S., Mazuski J. E., Baron E. J. et al. Guidelines for the selection of anti-infective agents for complicated intra-abdominal infections. Clin Infect Dis 2003; 37(4): 997–1005.
- Гельфанд Б. Р., Белоцерковский Б. З., Проценко Д. Н., Яковлев С. В., Еремин С. Р., Руднов В. А. и др. Нозокомиальная пневмония в хирургии: метод. рекомендации//Инфекции и антимикробная терапия. 2003. Т. 5. № 5–6.
- Сепсис в начале XXI века. Классификация, клинико-диагностическая концепция и лечение. Патологоанатомическая диагностика: практическое руководство. М.: Издательство НЦССХ им. А. Н. Бакулева РАМН, 2004. 130 с. Раздел «Антимикробная терапия сепсиса». Яковлев С. В., Сидоренко С. В., Зайцев А. А., Белобородов В. Б.
- Dennesen P. J., van der Ven J. A. M., Kessels A. G.et al. Resolution of infectious parameters after antimicrobial therapy in patients with ventilator-associated pneumonia. Am J Respire Crit Care Med. 2001; 163: 1371–1375.
С. В. Яковлев, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Приложения
-
- Современные подходы к антибактериальной терапии госпитальных инфекций - Таблица 1
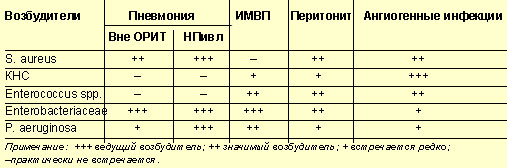
Ведущие бактериальные возбудители основных нозологических форм госпитальных инфекций









