Ацетилсалициловая кислота (АСК) на сегодняшний день представляет собой самое широко использующееся и, возможно, наиболее полно изученное лекарственное средство в мире. Тем не менее, несмотря на более чем 100-летний период, прошедший с момента ее создания, терапевтический потенциал и механизм действия АСК до конца не раскрыт.
В последние годы с позиций доказательной медицины выявлена польза назначения АСК самым разным категориям больных, однако спектр показаний для ее назначения по-прежнему расширяется, хотя не существует окончательного ответа на вопрос об оптимальных как с позиций эффективности, так и с позиций безопасности дозах АСК. Кроме того, не прекращаются попытки создания лекарственных форм, улучшающих переносимость АСК.
В настоящей статье рассматриваются основные группы пациентов, у которых назначение АСК позволяет снизить смертность и частоту серьезных сердечно-сосудистых осложнений при ишемической болезни сердца (ИБС), освещается вопрос о рекомендуемых в настоящее время дозах этого препарата, а также обсуждаются возможные пути повышения переносимости АСК. Общеизвестно, что применение АСК приводит к образованию язв и эрозий в верхних отделах желудочно-кишечного тракта, которые могут осложниться кровотечением. Менее известно негативное влияние АСК, даже кишечно-растворимых форм, на различные отделы кишечника. Наконец, самый часто встречающийся и на первый взгляд «безобидный» побочный эффект АСК — это диспепсия, однако именно по этой причине большинство больных прекращают прием препарата. Поэтому появление новых лекарственных форм АСК имеет не только научное, но и большое практическое значение.
Пациенты с острым инфарктом миокарда
Результаты мета-анализа Antithrom- botic Trialists’ Collaboration суммируют данные лечения 19 288 больных в 15 многоцентровых рандомизированных исследованиях, при этом средняя длительность лечения составила 1 мес. Назначение АСК в остром периоде ИМ позволило достоверно (p < 0,0001) снизить частоту сердечно-сосудистых событий на 38 на каждые 1000 леченных пациентов. Доказано, что среди 1000 больных острым ИМ прием АСК предотвращает 13 повторных нефатальных ИМ и 23 смерти от сердечно-сосудистых причин. При этом также достоверно (p < 0,02) снижается и частота инсультов — по 2 случая на каждые 1000 пациентов, получавших АСК (рис. 1).
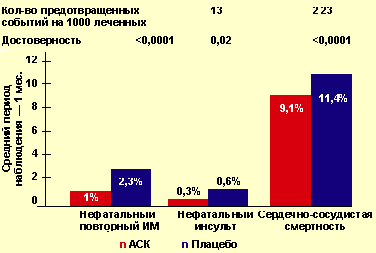 |
| Рисунок 1. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с острым инфарктом миокарда |
Наиболее крупным рандомизированным плацебоконтролируемым исследованием, включенным в мета-анализ Antithrombotic Trialists’ Collaboration, является ISIS-2. В нем приняли участие 17 187 больных из 16 стран, период наблюдения составил 35 дней. Целью исследования было сравнение эффективности терапии АСК 160 мг/сут, стрептокиназой 1,5 млн ЕД/ч, а также комбинированной терапии этими препаратами. Больные, которым не назначали ни АСК, ни стрептокиназу, составили контрольную группу.
Лечение АСК у пациентов с подозрением на острый ИМ приводило к уменьшению частоты развития нефатального повторного ИМ на 49%, инсульта на 46% (без увеличения риска геморрагического инсульта), сосудистой смертности на 23%. При этом АСК оказалась сопоставима с эффективностью стрептокиназы (смертность в течение 35 дней наблюдения снизилась, по сравнению с контрольной группой, соответственно на 25 и 23%). Эффективность АСК в острой стадии ИМ увеличивается при комбинации с тромболитиками до 42%. При этом, если комбинированная терапия начата в первые 6 ч после развития инфаркта, смертность уменьшается на 53%.
По данным ряда авторов, у пациентов, которые ранее, до развития ИМ, уже принимали АСК, ее назначение в острой стадии ИМ способствует более легкому течению инфаркта (при оценке по уровню ферментемии и по отсутствию зубца Q на ЭКГ). У пациентов, ранее не принимавших АСК, ее действие, в основном, проявляется увеличением уровня выживаемости.
Следовательно, назначение АСК в острой стадии ИМ позволяет достоверно увеличить выживаемость у этих больных уже через месяц лечения. Кроме того, наблюдение за 6213 из 17 187 участников, изначально включенных в исследование ISIS-2, показало, что увеличение выживаемости, достигнутое в первые месяцы, сохраняется по крайней мере еще в течение 10 лет. По мнению авторов данного исследования, прием АСК мог бы дать более положительные отдаленные результаты, если бы терапия не ограничивалась только 1 мес., а продолжалась бы длительнее.
Дополнительные благоприятные эффекты АСК в острой стадии ИМ обусловлены также ее анальгетическими и противовоспалительными свойствами. Так, было показано, что 1 г АСК, введенный внутривенно, препятствует развитию типичной ангинальной боли у 6 из 8 пациентов, у которых она была индуцирована введением брадикинина в левую венечную артерию. Это может оказаться очень важным патогенетическим механизмом, поскольку брадикинин высвобождается ишемизированной сердечной мышцей и может участвовать в формировании боли при ишемии миокарда.
В остром периоде ИМ для быстрого достижения антитромботического эффекта терапию всегда следует начинать с более высоких доз (от 160 до 325 мг), даже у пациентов, уже получающих по 75 мг препарата. Рекомендуют начинать терапию с «загрузочной дозы» в 500 мг.
Также АСК считается препаратом выбора при перикардите как одном из осложнений ИМ (ACC/AHA Guidelines, 1996).
Таким образом, назначение АСК в остром периоде инфаркта миокарда позволяет снизить сердечно-сосудистую смертность, риск развития повторного инфаркта миокарда и инсульта уже в ранние сроки (первый месяц текущего инфаркта миокарда). При этом указанное положительное влияние на прогноз сохраняется по меньшей мере в течение 10 лет. К дополнительным преимуществам АСК, назначаемой при остром инфаркте миокарда, следует относить ее анальгетический эффект, а также возможность лечения перикардита как осложнения инфаркта миокарда.
Пациенты с нестабильной стенокардией
АСК является препаратом первой линии в лечении больных с нестабильной стенокардией (острым коронарным синдромом), так как она снижает частоту развития сердечно-сосудистых смертей и ИМ.
Назначение АСК этой категории пациентов с ИБС сопровождается высокодостоверным (p < 0,0001) снижением риска серьезных сердечно-сосудистых осложнений на 46% (мета-анализ Antithrombotic Trialist’s Collaboration) (рис. 2). В мета-анализ включены результаты 12 рандомизированных исследований, в которых принимали участие более 5 тыс. пациентов с нестабильной стенокардией.
 |
| Рисунок 2. Снижение риска серьезных сердечно-сосудистых событий у различных групп пациентов с помощью применения АСК |
Как известно, у пациентов с нестабильной стенокардией тромбоциты находятся в активированном состоянии и регулярно высвобождаются вазоактивные медиаторы. Именно поэтому эффект АСК у данной категории пациентов выражен даже в большей степени, чем у пациентов со стабильной стенокардией.
Эффективность АСК в лечении больных нестабильной стенокардией была доказана рядом проспективных рандомизированных исследований. Так, в ходе проводившегося в госпитале ветеранов исследовании, целью которого являлось изучение влияния терапии АСК в суточной дозе 324 мг на частоту смерти и развития ИМ у больных с нестабильной стенокардией, включавшего более 1200 больных (период наблюдения составил 6 лет), было выявлено, что к третьему месяцу наблюдения у больных, получавших АСК, в сравнении с группой плацебо, суммарная частота смерти и ИМ снизилась на 41%, а еще через год она оказалась ниже на 43%. При этом различий между группами, касающихся частоты кровотечений, не было обнаружено.
Следует отметить, что профилактический (до развития клиники острого коронарного синдрома) прием АСК снижает частоту развития ИМ и смертность у больных с нестабильной стенокардией, а также уменьшает тяжесть клинических проявлений острой коронарной недостаточности.
В 1990 г. опубликованы результаты шведского исследования RISK, в ходе которого оценивали эффективность АСК в дозе 75 мг/сут в сравнении с плацебо. Через 3 и 12 мес. риск развития ИМ и смерти уменьшался на 48–64%, т. е. в 2,5-3 раза. Однако необходимо отметить, что, согласно данному исследованию, различия в летальности по сравнению с группой больных, получавших плацебо, стали проявляться не сразу, а только с третьего дня приема препарата, что было обусловлено низкой начальной дозой АСК. Поэтому в первые несколько дней с момента развития клиники нестабильной стенокардии или ИМ необходимо назначать АСК в дозе 325 мг/сут с последующим переходом на дозу 75–150 мг/сут.
Пациенты с инфарктом миокарда в анамнезе
Мета-анализ Antithrombotic Trialists’ Collaboration охватил 11 многоцентровых плацебоконтролируемых исследований, в которых приняли участие в общей сложности 18 788 больных, а средний срок наблюдения составлял 27 мес. Полученные результаты с высокой степенью достоверности (p < 0,0001) свидетельствуют о снижении риска сердечно-сосудистых событий (инфаркт миокарда + инсульт + сердечно-сосудистая смертность) на фоне лечения АСК(рис. 3). Так, назначение АСК позволяет предотвратить 36 серьезных сердечно-сосудистых эпизодов, в том числе 18 повторных нефатальных ИМ, 14 смертей от сердечно-сосудистых причин и 5 нефатальных инсультов на каждую 1000 пациентов. Показано, что назначение АСК в течение длительного времени после перенесенного ИМ снижает смертность на 31%, частоту повторного нефатального ИМ также на 31%, частоту нефатального инсульта — на 42%. Поэтому все пациенты с инфарктом миокарда в анамнезе должны получать АСК в дозе 75–150 мг/сут.
 |
| Рисунок 3. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с инфарктом миокарда в анамнезе |
Пациенты со стабильной стенокардией
Согласно данным мета-анализа Antithrombotic Trialist’s Collaboration, назначение АСК пациентам со стабильной стенокардией сопровождается высокодостоверным (p = 0,00004) 33-процентным снижением риска серьезных сердечно-сосудистых событий (ИМ + инсульт + сердечно-сосудистая смертность) (рис. 2). В мета-анализ включены результаты 7 рандомизированных исследований, в которых принимали участие около 3 тыс. пациентов со стабильной стенокардией.
По данным исследования, проведенного в 1991 г. американскими врачами, в котором приняли участие 333 мужчин со стабильной стенокардией без ИМ и инсульта в анамнезе (период наблюдения — 5 лет, доза АСК — 325 мг через день), снижение частоты первичных ИМ на фоне терапии АСК составило 87%.
В шведском рандомизированном, двойном слепом и плацебоконтролируемом исследовании SAPAT, включавшем 2035 больных со стабильной стенокардией, период наблюдения составил в среднем 50 мес. Все больные принимали b-блокатор соталол в средней дозе 160 мг, АСК назначали в дозе 75 мг/сут. В группе АСК, по сравнению с плацебо, отмечено достоверное снижение частоты ИМ и внезапной смерти на 34%, а частота сосудистой смерти, инсультов и общая смертность снизились на 22–32%.
По данным некоторых авторов, у лиц, принимающих АСК и госпитализирующихся в связи с приступом стенокардии, ИМ без зубца Q на ЭКГ развивается с относительно меньшей вероятностью.
Пациенты с «немой» ишемией миокарда
АСК не менее эффективна при «немой» ишемии миокарда, чем при симптоматическом варианте ИБС. По данным некоторых сравнительных рандомизированных исследований, в ходе которых пациенты с «немой» или симптоматической ишемией миокарда ежедневно получали 75 мг АСК либо плацебо, в группе больных с «немой» ишемией миокарда за 3 мес. наблюдения благодаря приему АСК риск развития ИМ снизился более чем на 80% по сравнению с плацебо (4 против 21%). В то же время у пациентов с клинически выраженными симптомами стенокардии риск ИМ по сравнению с плацебо уменьшился вдвое (9 против 21%).
Пациенты после операции на коронарных артериях
Польза от назначения АСК этой категории больных несомненна. Дело в том, что все эти методы лечения неизбежно связаны с повреждением эндотелия и последующей активацией тромбоцитов. АСК подавляет активацию тромбоцитов, таким образом препятствуя развитию раннего стенозирования стента или рестенозирования коронарных сосудов (Antiplatelets Trialists’ Collaboration II, 1994).
По данным мета-анализа Antithrombotic Trialists’ Collaboration (2002), у больных после коронарной ангиопластики назначение АСК сопровождается 53-процентным снижением риска серьезных сердечно-сосудистых осложнений (p < 0,0001) (рис. 2). В мета-анализ включены результаты 9 рандомизированных исследований, в которых приняли участие более 3 тыс. пациентов. Результаты применения АСК у больных после аортокоронарного шунтирования выглядят скромнее — снижение риска серьезных сердечно-сосудистых осложнений всего на 4% (данные 25 рандомизированных исследований, более 6 тыс. пациентов).
Терапию АСК предпочтительно начинать вечером накануне хирургического вмешательства или (как вариант) сразу после него. При более позднем начале терапии (через 3 дня после аортокоронарного шунтирования) АСК, как и непрямые антикоагулянты, не предупреждали окклюзии венозных шунтов. Оптимальной дозой для длительного приема после оперативных вмешательств считают 100–160 мг/сут. В настоящее время все большее распространение получает тенденция комбинирования АСК с другими антиагрегантными препаратами.
Несмотря на явную пользу от применения АСК при ИБС, ее использование в реальной клинической практике ограничено из-за побочных эффектов. Помимо риска кровотечений, который повышен у пожилых пациентов, при одновременном приеме кортикостероидов, а также при наличии язвенной болезни в анамнезе основной клинической проблемой, препятствующей назначению АСК, становятся частые побочные явления со стороны желудочно-кишечного тракта — прежде всего эрозивно-язвенные поражения желудочно-кишечного тракта и диспептические симптомы.
Возникновение эрозивно-язвенных поражений желудка на фоне приема АСК даже в дозах, применяемых в кардиологии, представляет собой общеизвестный факт. Эти язвы можно эффективно лечить теми же препаратами, что и язвенную болезнь. Как правило, рубцевание язвы происходит быстрее, если АСК отменена, при этом условии сроки рубцевания аналогичны срокам рубцевания при язвенной болезни — на четвертой–восьмой неделе лечения. Однако, если терапию АСК продолжать, несмотря на выявленное эрозивно-язвенное поражение желудочно-кишечного тракта, показатели рубцевания становятся достаточно удовлетворительными: к четвертой неделе лечения рубцуются 60–75% язв.
Долгое время единственным и практически 100-процентным решением этой проблемы многие считали применение кишечно-растворимых форм АСК. Однако ряд авторов отметили образование эрозий и язв желудка даже при применении таблеток АСК, покрытых кишечно-растворимой оболочкой. Более того, согласно результатам еще одного исследования, применение кишечно-растворимых форм АСК у пациентов с аспирин-индуцированными язвами не вело к увеличению показателей рубцевания язв при терапии циметидином и антацидами; у 7 больных, получавших АСК в кишечно-растворимой оболочке, вообще не удалось достичь рубцевания язвы, тогда как у 90% больных после отмены этой формы АСК язвы зарубцевались.
Поэтому сегодня созданы новые лекарственные формы АСК, предлагающие другие способы защиты желудочно-кишечного тракта. Особый интерес представляет препарат кардиомагнил: соединение АСК (в наиболее эффективных и безопасных дозах — 75 и 150 мг) с невсасывающимся антацидом — гидроокисью магния.
Невсасывающиеся антациды наиболее часто используются для лечения заболеваний желудка, в том числе и язвенной болезни. Свой положительный эффект они реализуют, адсорбируя соляную кислоту. Кроме того, невсасывающиеся антациды обладают и рядом других позитивных свойств. Они снижают протеолитическую активность желудочного сока (посредством адсорбции пепсина, повышения pH среды, в результате чего пепсин становится неактивным), обладают обволакивающими свойствами, связывают лизолецитин и желчные кислоты, оказывающие неблагоприятное воздействие на слизистую желудка.
Но, пожалуй, наиболее важны для профилактики аспирин-индуцированных осложнений данные о цитопротективном действии антацидов, опубликованные в последние годы. В частности, о том, что антациды способны предотвращать в экспериментальных и клинических условиях возникновение повреждений слизистой оболочки желудка при применении нестероидных противовоспалительных препаратов. Было установлено, что цитопротективный эффект антацидов обусловлен повышением уровня простагландинов в стенке желудка (снижение уровня простагландинов в стенке желудка — основной механизм язвообразования при применении АСК), усилением секреции бикарбонатов и увеличением гликопротеинов желудочной слизи.
Гидроокись магния, входящая в состав кадиомагнила, кроме того, является наиболее быстродействующим антацидом, в отличие от гидроокиси алюминия. Это очень важный момент, поскольку АСК быстро всасывается из желудка: значимые концентрации в плазме достигаются всего через 15–20 мин. При этом результаты специально проведенных исследований показали, что гидроокись магния не влияет на всасываемость АСК.
Наконец, самым распространенным побочным эффектом АСК со стороны желудочно-кишечного тракта является диспепсия (по данным некоторых авторов, на ее долю приходится 50% и более случаев), причем эзофагогастродуоденоскопия не выявляет эрозивно-язвенных и воспалительных изменений. Этот вроде бы безобидный симптомокомплекс служит наиболее частой причиной отказа пациента от приема АСК. Соединение АСК с гидроокисью магния позволит резко снизить частоту диспепсии и повысить приверженность пациентов к лечению.
О. Д. Остроумова, доктор медицинских наук, профессор МГМСУ, Москва









