Какова физиологическая роль магния в организме?
Каков механизм нейропротективного действия магния?
Почему клинические результаты использования магния у больных с инсультом хуже, чем лабораторные? Многолетний поиск нейропротективных агентов, т. е. препаратов, уменьшающих степень повреждения мозговых структур при острой ишемии, не привел к однозначным результатам. Более того, из-за разнообразия препаратов и рекомендаций по их применению смысл термина «нейропротекция» сделался расплывчатым. Да и сама связь действия ряда лекарственных веществ с заявленной нейропротекторной активностью представляется порой трансцендентальной — настолько нечетко бывает изложен механизм их действия.
Общие свойства магния
Среди препаратов-«долгожителей» можно упомянуть магний. Лечение солями магния практикуется давно, но вплоть до 70-х гг. прошлого века они рассматривались как слабительное, реже как гипотензивное или спазмолитическое средство.
Изучение распределения магния в организме показало, что основное его количество депонировано в костях. Внутри клеточных структур магний на 95—98% связан с АТФ.
Внутриклеточное содержание не связано напрямую с общим содержанием магния в организме и с его сывороточной концентрацией (в норме от 0,7 до 1,1 ммоль/л). Концентрация магния в спинно-мозговой жидкости, напротив, коррелирует с его сывороточной концентраций и на 15—20% превышает последнюю.
Открытие тонкой структуры внутриклеточных ионных токов и взаимодействий позволило несколько по-иному оценить роль, которую магний играет в организме. Была обнаружена его способность связываться с АТФ, участвовать в ряде цитохимических реакций, регулировать цикл сокращение/расслабление в мышце. Наконец, выяснилось, что магний способен конкурировать с ионами кальция как на уровне трансмембранного переноса, так и на уровне внутриклеточных взаимодействий.
Описанные свойства определили новую область применения препаратов магния — речь идет о лечении заболеваний, сопровождающихся ишемическим повреждением тканей.
Теоретическим обоснованием применения магния при ишемии является его способность модулировать различные этапы каскада ишемического повреждения клеток.
В частности, развитие острой ишемии головного мозга приводит к быстрому формированию зоны некроза в тех участках, кровоток в которых падает до уровня менее 1 мл/10 г/мин. Естественно, спасти клетки в этой зоне может только вмешательство, направленное на неотложное восстановление кровотока (тромболитическая терапия).
В то же время по периферии некротического очага формируется так называемая зона ишемического риска (кровоток от 1 до 2 мл/10 г/мин), в отношении которой прогноз не может быть столь определенным. Клетки, находящиеся в этой зоне, подвергаясь воздействию ишемии, могут сами запускать процессы, результатом которых будет дальнейшее расширение зоны некроза.
В первую очередь речь идет о так называемой эксайтотоксичности (от английского to excite — возбуждать). Развивающийся в ишемизированной ткани лактоацидоз (следствие перехода на анаэробный путь утилизации глюкозы) приводит к массивному выбросу глутамата и аспартата, связывающихся с постсинаптическими N-метил-D-аспартат-рецепторами нервных клеток. Активация последних способствует повышению проницаемости мембраны и массивному вхождению внутрь клетки ионов кальция. Дальнейшие события обусловлены эффектом кальциевой перегрузки — запуск процессов образования свободных радикалов, повреждение последними липидов мембран. Все это приводит к развитию системного воспалительного ответа, в ходе которого ткани, находящиеся в состоянии критической ишемии, подвергаются дальнейшему повреждению.
Наконец, ионная перегрузка приводит к «пробуждению» генов, ответственных за развитие процесса апоптоза (т. е. процесса запрограммированного самоуничтожения клетки).
В эксперименте ионы магния демонстрируют антиэксайтотоксический эффект — они способны подавлять высвобождение глутамата, а также вступать с ним в неконкурентный антагонизм на уровне NMDA рецепторов.
Магний вступает в антагонизм с ионами кальция как на уровне мембранных каналов, так и внутри клетки. Повышенное содержание внутриклеточного магния приводит к повышенной буферизации кальция внутри митохондрий, а также препятствует истощению клеточных запасов АТФ.
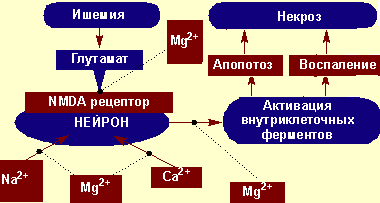
Схематическое представление феномена эксайтотоксичности, а также место ионов магния в его подавлении отображены на рисунке 1.
| Фуномен эксайтотоксичности и роль ионов магния в его предупреждении. |
 |
Кроме воздействия на клеточном уровне ионы магния проявляют и другие свойства. Магний улучшает мозговой кровоток путем непосредственного воздействия на тонус сосудов, а также в результате антагонизма к эндотелину-1. Кроме того, он обладает противосудорожной активностью и системным гипотензионным эффектом.
Антиагрегантная активность ионов магния, доказанная в ходе экспериментов, позволяет обсуждать возможные механизмы потенцирования эффектов аспирина и тромболитиков, что также немаловажно для лечебного вмешательства при ишемии.
Те же самые свойства делают возможным применение магния и при мозговых кровоизлияниях. Магний препятствует развитию ангиоспазма и срыву интракраниальной сосудистой ауторегуляции, нормализует повышенное артериальное давление, блокирует нейромышечную трансмиссию и предотвращает развитие судорог, препятствует развитию отека мозга и повышению внутричерепного давления.
Фармакокинетические исследования, проводимые при лечении пациентов с пре-эклампсией, показали, что лечебный эффект магния отмечается при превышении обычной сывороточной концентрации в полтора-два с половиной раза. Такая концентрация достаточно безопасна, так как нарушение нейромышечной передачи и даже угнетение дыхания наступают при концентрации от 3,5 мг и выше. Следует учитывать также тот факт, что период полувыведения магния при сохраненной функции почек равен 3,5—4 ч.
Таким образом, оптимальным режимом введения магния при острых ишемических событиях является внутривенное введение нагрузочной дозы с целью создания требуемой терапевтической концентрации с последующей пролонгированной инфузией.
Применение подобного режима введения в ряде экспериментальных работ на животных привело к снижению объема некроза при моделированном инфаркте мозга на 25—65%. В экспериментальных работах использовались как сульфат, так и хлорид магния, однако гипергликемия, развивающаяся при введении последнего, дает основание думать, что оптимальным соединением для внутривенного введения является сульфат магния.
В более поздних работах показано не только влияние на объем поражения, но и на исходы (смерть или развитие стойкого двигательного дефицита) у лабораторных животных.
Количество проведенных на людях исследований, посвященных возможности применения магния при инсульте, невелико, хотя бы по сравнению с исследованиями воздействия магния при инфаркте миокарда, в которых за последние 20 лет приняли участие более 70 тыс. пациентов. Те же исследования при инсульте включают немногим более 1000 пациентов. Негомогенность этих изысканий делает невозможным проведение метаанализа. Результаты же всех имеющихся экспериментов показывают, что применение сульфата магния определяет тенденцию к улучшению прогноза после перенесенного инфаркта мозга. Справедливости ради надо заметить, что практически во всех опубликованных работах статистически значимое снижение частоты исходов было не отмечено.
Отдельного обсуждения заслуживает проблема как можно более раннего назначения нейропротекторных агентов при инсульте.
Каскад эксайтотоксичности развивается сразу после наступления инсульта, и каждый час отсрочки существенно ухудшает прогноз. Практически все лабораторные эксперименты предусматривали раннее (в течение 1-2 ч) введение препаратов магния. В то же время в клинических исследованиях этот срок составлял от 4 до 48 ч. Этим во многом объясняются различия между многообещающими лабораторными и довольно скромными клиническими результатами.
Так как фактор времени является определяющим, правомерно поставить вопрос о возможности применения препаратов магния на догоспитальном этапе. В 2002 г. были опубликованы результаты пилотного исследования FAST-MAG, в ходе которого предварительная диагностика инсульта проводилась парамедиками. Они же начинали лечение сульфатом магния, которое затем продолжалось на стационарном этапе. Результаты оказались обнадеживающими — в группе пациентов, получавших сульфат магния, было выявлено снижение частоты наступления комбинированной точки (смерть или стойкий неврологический дефицит на 90-й день). Кроме того, отмечалась существенное ускорение начала введения сульфата магния — в среднем 23 мин против 2 ч от момента поступления в стационар (как это было в предшествующих исследованиях). В настоящее время планируется проведение дальнейших исследований в этой области.
В следующем году станут доступны результаты проводящегося в настоящее время исследования IMAGES. Исследование должно охватить более 5000 пациентов с инсультом (не более 12 ч от момента развития), половина из которых будут получать плацебо, а половина — сульфат магния по наиболее распространенной схеме: болюсное введение 1 г с последующей суточной инфузией 8 г. На 30-е и 90-е сутки будет оцениваться соотношение летальности и уровня стойкого двигательного дефицита в группах вмешательства. Планируется достижение абсолютной разницы в 5,5% за счет улучшения прогноза в группе пациентов, которым будет назначен сульфат магния.
Заключение
Таким образом магний является многообещающим нейропротекторным агентом. Результаты преклинического тестирования этого препарата отчасти превосходят результаты преклинического тестирования других нейропротекторов. В то же время проблема своевременного назначения препаратов магния может быть решена путем активного внедрения его в схемы догоспитальной помощи больным с инсультом.
Многочисленные исследования, проведенные в последние 20 лет, продемонстрировали отсутствие у магния значимых побочных эффектов. А безопасность препарата определяет возможность его применения не только врачебными, но и фельдшерскими бригадами.
Кроме того, у препаратов магния не выявлено каких-либо значимых взаимодействий с другими лекарственными веществами, применяющимися для лечения инсульта (необходимо лишь помнить о возможном потенцировании гипотензивного эффекта).
Одним из перспективных терапевтических подходов является применение препаратов магния не только в виде инфузионной нагрузки в период непосредственного развития сосудистой кататстрофы, но и применение таблетированных форм, таких как оротат магния (магнерот) как с целью профилактики (пополнение запасов магния в депо), так и с целью продолжения лечения магнием по окончании его внутривенной инфузии.
А. Л. Верткин, доктор медицинских наук, профессор
О. Б. Талибов, кандидат медицинских наук
И. А. Измайлов
ННПОСМП МГМСУ, Москва
.jpg)
.jpg)
.jpg)











