Инфекции дыхательных путей остаются серьезной проблемой клинической медицинской практики в связи с их широкой распространенностью и наносимым экономическим ущербом, как отдельным лицам, так и обществу в целом. Хотя большинство острых респираторных заболеваний (ОРЗ) имеет легкое течение и не дает осложнений, они ухудшают самочувствие детей, препятствуют их повседневной активности.
В структуре инфекционной заболеваемости на долю ОРЗ приходится от 60 до 90% всей детской инфекционной заболеваемости [1, 2]. Они регистрируются повсеместно и в любое время года, но массовый характер приобретают во время сезонного подъема заболеваемости с октября по март. В популяции детей выделяют диспансерную группу часто и длительно болеющих респираторными заболеваниями, доля которых составляет от 20 до 75%. Эта группа детей имеет более высокий (> 60% всех заболеваний детского возраста) уровень заболеваемости [5, 6]. Многочисленные исследования указывают на то, что значительная доля детей с рецидивирующей респираторной патологией имеет фоновые аллергические заболевания (атопический дерматит, аллергический ринит, бронхиальная астма). В ряде исследований показано, что у часто болеющих детей на фоне дефицита факторов инфекционной защиты происходит формирование повышенной чувствительности рецепторного аппарата бронхов и увеличение уровня специфического иммуноглобулина (Ig) E к вирусам и бактериям [3].
Последствиями рецидивирования респираторных заболеваний могут быть нарушения физического и нервнопсихического развития, что способствует снижению функциональной активности иммунной системы и формированию хронических воспалительных процессов в органах дыхания. В последнее десятилетие устойчиво сохраняется тенденция к росту респираторной патологии во всех возрастных группах детей, что требует проведения мер действенной первичной и вторичной профилактики. Разработка эффективных профилактических и лечебных мероприятий для детей c респираторной патологией представляет не только медицинскую, но и социальную проблему. Для каждого ребенка необходим индивидуальный подход, включающий комплексную программу профилактики, лечения и реабилитации с учетом этиологических и патогенетических механизмов заболевания, а также комплекса факторов внешнего окружения, формирующих предрасположенность организма ребенка к частым респираторным заболеваниям. Программа профилактики и реабилитации детей с заболеваниями респираторной системы должна быть интегрирована во все звенья социума ребенка (семья, дошкольное образовательное учреждение, школа, поликлиника, санаторий). В профилактический раздел программы помимо собственно профилактических мероприятий, направленных на предупреждение заболеваний и укрепление здоровья детей, должны включаться и лечебные воздействия, направленные на коррекцию выявленных в состоянии здоровья отклонений. При этом большое значение имеет повышение устойчивости организма ребенка с помощью иммуномодулирующих препаратов. Появление в последнее время иммунотропных средств нового поколения создает предпосылки их целенаправленного применения с целью коррекции иммунного статуса и функционального состояния организма в целом.
Общие профилактические мероприятия программы оздоровления часто болеющих детей с атопией включают оптимизацию режима дня и различные виды закаливающих процедур, внедрение рационального режима двигательной активности ребенка, сбалансированное, соответствующее возрасту и функциональным возможностям пищеварительных желез питание.
Профилактический комплекс фармакологической коррекции подбирается в зависимости от нозологической формы патологии, возраста ребенка и его индивидуальных особенностей. Как правило, основу такого комплекса составляют индивидуальные схемы вакцинопрофилактики, профилактические курсы интерферонов или их индукторов, фитотерапия, физиосветолечение. По показаниям возможно включение в программу оздоровления собственно противовирусных средств, бактериальных лизатов, препаратов иммунокорригирующего действия.
В настоящее время эффективные и безопасные вакцины разработаны против нескольких респираторных патогенов, таких как вирус гриппа, пневмококк и гемофильная палочка [4]. Однако необходимо иметь в виду, что возможности вакцинопрофилактики респираторных инфекций у часто болеющих детей с атопией могут быть ограничены, что обусловлено особенностями формирования и течения атопических заболеваний на фоне реализации «аллергического марша» [4–7]. Поэтому лечащий врач должен более тщательно подходить к вакцинации данной категории детей. С точки зрения безопасности и эффективности у детей с рецидивирующей респираторной патологией и атопией целесообразно использовать инактивированные вакцины: расщепленные или сплит-вакцины (Ваксигрип, Бегривак, Флюарикс) и субъединичные (Гриппол, Инфлювак, Агриппал). Субъединичные и большая часть сплит-вакцин разрешены для использования у детей с 6-месячного возраста.
Вторым направлением всех профилактических программ является использование интерферонов (ИФН), как наиболее значимых факторов собственной противовирусной защиты организма ребенка, а также индукторов ИФН. Система интерферонов формирует защитный барьер намного раньше специфических иммунных реакций, обеспечивая резистентность к широкому спектру возбудителей острых респираторных вирусных инфекций (ОРВИ) и оказывая влияние на последующий, собственно иммунный ответ. Кроме того, интерфероны оказывают иммуномодулирующее действие. Антивирусные свойства в большей степени выражены у ИФН α и ИФН β, в то время как иммунорегуляторные и антипролиферативные — у ИФН γ. Важно отметить, что ИФН γ подавляет Тh2-ответ, что способствует лучшему контролю инфекционно-аллергического воспалительного процесса в респираторной системе [5–7]. Именно у детей с атопией, в имунной системе которых имеется нарушение баланса Тh1- и Тh2-активностей, перспективно применение препаратов, активизирующих ИФН γ.
В настоящее время в арсенале педиатров имеются препараты интерферонов природного происхождения — человеческий лейкоцитарный интерферон (Локферон, Лейкинферон) и рекомбинатные интерфероны (Виферон, Гриппферон). В последние годы для лечения и профилактики респираторных инфекций все чаще применяются рекомбинатные ИФН, что объясняется их более высокой активностью и безопасностью. В основном препараты ИФН содержат различные виды ИФН α. Наиболее широко в педиатрической практике применяется Виферон (рекомбинатный ИФН α-2), обладающий антиоксидантным эффектом за счет входящих в его состав витаминов С и Е.
Вместе с тем в группе часто болеющих детей с атопией предпочтительнее применять индукторы эндогенного интерферона. Тем самым удается избежать дополнительной сенсибилизации детей с атопией, поскольку рекомбинантные интерфероны могут обладать определенной антигенной чужеродностью. Кроме того, при использовании индукторов интерферона синтез индуцированного ИФН находится под контролем самого организма.
Наиболее широко известными синтетическими индукторами интерферона являются производные тилорона (Амиксин) и Циклоферон. Кроме того, эффектом стимуляции образования ИФН в организме обладает Арбидол. При применении классических индукторов эндогенного интерферона в основном стимулируется продукция ИФН α/β различными клетками организма. В отличие от классических индукторов интерферона, Анаферон, содержащий сверхмалые дозы антител к ИФН γ, индуцирует и модулирует продукцию не только ИФН α/β, но и ИФН γ [8]. Благодаря этому Анаферон способствует восстановлению баланса Th1- и Th2-активностей в организме [8], что особенно важно для применения у больных с атопией. Следует отметить, что практически все представленные препараты не только индуцируют синтез эндогенного интерферона, но и оказывают выраженное влияние на иммунную систему (стимулируют фагоцитоз и клеточный иммунитет), а некоторые обладают прямым противовирусным действием (Амиксин, Арбидол). При выборе конкретного препарата необходимо обращать внимание не только на его фармакологическую активность, но и на возрастные ограничения. Так, Анаферон детский разрешен к применению, начиная с 6-месячного возраста, Арбидол может быть использован у детей старше 2 лет, Циклоферон разрешен у детей старше 4 лет, а Амиксин — только у детей старше 7 лет.
ОРВИ оказывают влияние на формирование атопического заболевания и зачастую являются фактором, вызывающим обострение заболевания [3, 5]. Рациональная тактика ведения детей, страдающих атопическими заболеваниями, предусматривает длительную (желательно — многомесячную) профилактику респираторных инфекций. С учетом того, что Анаферон содержит сверхмалые дозы действующего вещества, следует ожидать, что он не оказывает истощающего влияния на иммунную систему детей с атопией, а также у детей из группы часто болеющих при длительном применении (рекомендуемая продолжительность профилактических курсов Анаферона — 3 мес).
Профилактическая и лечебная эффективность Анаферона детского по отношению к ОРВИ неоднократно исследовалась не только в группах здоровых детей, но и среди детей, страдающих атопическими заболеваниями, а также у детей, относящихся к группе часто болеющих [8–17].
В рандомизированных открытых сравнительных исследованиях, проведенных в Москве (В. А. Ревякина и соавт.) [12] и на кафедре детских болезней № 3 ЧГМА (Челябинск) [13], исследовали профилактическую и лечебную эффективность Анаферона детского по отношению к ОРВИ у детей в возрасте от 1 года 8 мес до 7 лет с бронхиальной астмой, атопическим дерматитом и аллергическим ринитом. Поскольку в исследование входили часто болеющие дети с атопическими заболеваниями, Анаферон назначался максимально продолжительным курсом — на 3 мес. В общей сложности Анаферон получали 93 ребенка (основная группа). Дети из группы сравнения (51 ребенок), в соответствии с протоколом, не получали иммуномодулирующие препараты в течение всего периода наблюдения. Согласно полученным данным, разница в показателях заболеваемости (среднее групповое число случаев ОРВИ) в обеих группах при оценке в разные периоды наблюдения колебалась в пределах от 3 до 1,5. За 6 мес наблюдения дети основной группы болели в 1,8 раз реже, чем дети группы сравнения. Применение Анаферона с лечебной целью у детей, с развившейся ОРВИ, способствовало снижению тяжести течения заболевания и частоты развития осложнений. При этом отмечалось позитивное влияние Анаферона на систему интерферонов. При исследовании интерферонового статуса был отмечен рост уровня индуцированной продукции интерферонов в основной группе (ИФН γ — в 1,4 раза и ИФН α — в 1,3 раза), в то время, как в группе сравнения указанные показатели значимо не изменялись.
Следует отметить, что уровень спонтанной продукции ИФН, исследуемый на фоне длительного приема Анаферона, не изменялся, что свидетельствует о физиологическом характере влияния Анаферона на систему ИФН у детей с атопией, поскольку прием Анаферона влиял лишь на индуцированную продукцию ИФН, т. е. увеличивал функциональные резервы данной системы.
С учетом высокой значимости специфической иммунопрофилактики гриппа у детей с разнообразной аллергологической патологией заслуживают внимания данные, полученные в сравнительном рандомизированном двойном слепом плацебо-контролируемом исследовании эффективности индукторов эндогенного интерферона в качестве подготовки к проведению вакцинации у детей с рецидивирующими инфекциями верхних дыхательных путей, проведенном сотрудниками кафедры педиатрии РМАПО [17]. По данным авторов, проведение профилактического курса Анаферона детского, начатое в предвакцинальный период (за 10–14 дней до предполагаемой вакцинации), позволяет увеличить долю детей, вакцинированных от гриппа, за счет снижения заболеваемости ОРВИ в 1,6 раза. Кроме того, в данной работе были получены свидетельства положительного влияния Анаферона на результаты самой вакцинации часто болеющих детей раннего возраста. Так, доля детей, имеющих защитные титры антител к актуальному штамму вируса гриппа А (H1N1) (А/Новая Каледония/20/99), в основной группе выросла после вакцинации в 3,9 раза (с 17% до 67%), в то время как в группе сравнения доля детей с защитными титрами изменилась лишь в 1,3 раза (с 28 до 36%). Аналогичные изменения, более или менее выраженные, были отмечены и по отношению к другим вакцинальным штаммам.
Следовательно, применение индукторов ИФН в предвакцинальный период позволяет увеличить охват прививками против гриппа, а проведение ослабленным и часто болеющим детям раннего возраста вакцинации против гриппа на фоне неспецифической иммунопрофилактики Анафероном детским является перспективным в виду более высокой иммунологической эффективности. Очевидно, что опыт подготовки часто болеющих детей к вакцинации против гриппа нуждается в дальнейшем изучении и возможно его следует использовать при проведении вакцинации детей с атопической патологией.
В течение последнего времени мы также исследуем возможности применения Анаферона детского у больных с БА для профилактики и лечения ОРВИ, а значит, и для контроля над течением основного заболевания. Наблюдение осуществлялось за 113 детьми в возрасте от 12 мес до 7 лет, имеющими верифицированный диагноз БА различной степени тяжести. С помощью рандомизации были сформированы основная (n = 58 детей, прием Анаферона в течение 3 мес) и контрольная (n = 55, не получали иммуномодуляторы) группы. Сравниваемые группы были репрезентативны по тяжести основного заболевания и возрасту (табл. 1). Базисная терапия астмы проводилась в соответствии с тяжестью течения и была сопоставимой в группах сравнения. В случае развития ОРВИ детям обеих групп проводилась традиционная терапия ОРВИ, а дети основной группы дополнительно получали Анаферон по лечебной схеме.
В результате исследования выявлено, что в основной группе среднее число случаев ОРВИ было значительно ниже, чем в контрольной (0,36 ± 0,09 против 1,06 ± 0,15, p < 0,0001).
Назначение Анаферона в ранние сроки заболевания детям, у которых за период наблюдения развились ОРВИ, способствовало более быстрой ликвидации всех проявлений инфекционного процесса (табл. 2).
Таким образом, профилактическое использование Анаферона детского обеспечивает снижение заболеваемости ОРВИ почти в 3 раза. Отсутствие детей в организованных детских коллективах в связи с ОРВИ по поводу одного случая в основной группе составило в среднем 4,9 ± 1,12 дня, в контрольной группе — 7,3 ± 1,22 (р < 0,05).
Частота обострений БА в обеих группах представлена на рис. В основной группе у 8% детей были зарегистрированы за период наблюдения однократные обострения БА. У двух детей со среднетяжелой формой БА, требующей применения Фликсотида, были отмечены случаи повторного обострения в виде появления легких признаков бронхиальной обструкции, быстро купировавшихся при использовании Беродуала. При этом не возникало необходимости изменять базисную терапию. Обострений сопутствующих аллергических заболеваний на фоне ОРВИ в основной группе отмечено не было.
В контрольной группе за время наблюдения у 28 детей (50,9%) были зарегистрированы признаки БА, в том числе половина из них была госпитализирована, при выписке из стационара им была переоценена тяжесть БА и увеличен объем базисной терапии с переходом на ингаляционные глюкокортикостероиды. У 14 пациентов присоединение бактериальной инфекции потребовало назначение антибиотиков. В этой группе помимо клиники БА отмечалось появление симптомов атопического дерматита у 8 детей, аллергического ринита — у 6. Таким образом, помимо более выраженных и затяжных проявлений ОРВИ у пациентов контрольной группы отмечались обострения всех аллергических заболеваний, более частые бактериальные осложнения, что существенно увеличивало объем и длительность фармакотерапии, в том числе требовалось усиление базисной терапии БА.
В ходе исследования мы отметили, что Анаферон детский имеет высокий профиль безопасности и хорошо переносится детьми с атопией, в частности с БА и атопическим дерматитом.
Таким образом, необходимо использовать дифференцированные подходы к профилактике вирусной респираторной патологии у больных с атопией. Различие профилактических подходов должно определяться, прежде всего, возрастными особенностями детского организма, фармакологическими характеристиками лекарственных препаратов, а также влиянием микросоциальных факторов внешнего воздействия и возможностями объема медико-профилактической помощи медицинского или образовательного учреждения. Целесообразно включать Анаферон в программы профилактики респираторной патологии у детей с атопией.
Практикующие врачи, педагоги и воспитатели образовательных учреждений, родители часто болеющих детей с атопическими заболеваниями должны помнить, что только последовательные и комплексные профилактические мероприятия в течение 2–3 лет подряд приведут к заметному снижению частоты заболеваний и улучшению качества жизни этой категории пациентов.
По вопросам литературы обращайтесь в редакцию.
А. Б. Малахов, доктор медицинских наук, профессор
Е. Г. Кондюрина, доктор медицинских наук, профессор
Т. Н. Елкина, доктор медицинских наук, профессор
В. А. Ревякина, доктор медицинских наук, профессор
ММА им. И. М.Сеченова, Москва
Новосибирский ГМУ, Новосибирск
НЦЗД РАМН, Москва
Приложения
-
- Современные аспекты профилактики респираторных инфекций у детей с атопией - Таблица 1
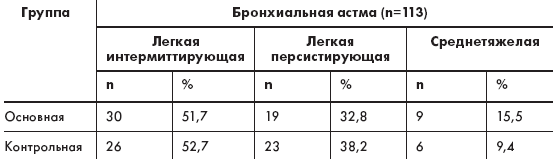
Структура степени тяжести бронхиальной астмы у наблюдаемых детей
-
- Современные аспекты профилактики респираторных инфекций у детей с атопией - Таблица 2

Продолжительность клинических проявлений у наблюдаемых детей









