В основе ведущих метаболических процессов человека лежат окислительно-восстановительные реакции. Среди них особую роль играют свободнорадикальные реакции, при которых в результате метаболических процессов образуются перекисные соединения. Инициатором образования таких соединений обычно являются свободные радикалы — молекулы или фрагменты молекул, имеющие в одном из атомов кислорода неспаренный электрон. Активные формы кислорода чаще всего представлены супероксидным (О2о) и гидроксипероксидным (НО2о) радикалами.
Указанные радикалы вступают во взаимодействие между собой с образованием перекиси водорода либо могут непосредственно окислять органические молекулы (жирных кислот, участки белковых комплексов) с образованием свободнорадикальных фрагментов таких молекул или перекисных соединений: RH+ HO2--> H2O2+Ro, образующих новые радикалы и гидроперекиси, Ro+O2->ROOo->ROOH+Ro распад которых также ведет к появлению радикалов ROOH-> RO0+ OH- [1, 2]; т. e. при отсутствии реакции обрывания цепи процессы свободнорадикального окисления могут приобрести лавинообразный, неконтролируемый характер.
Одним из основных субстратов для свободнорадикальных реакций служат липиды, в первую очередь молекулы полиненасыщенных жирных кислот (ЖК), липидные компоненты липопротеидов низкой и очень низкой плотности (ЛОНП и ЛНП). В результате окисления ЖК образуются гидроперекиси (диеновые конъюгаты), которые затем метаболизируются во вторичные — малоновый диальдегид (МДА) и третичные продукты перекисного окисления липидов (ПОЛ) — шиффовы основания. Процессы ПОЛ протекают во всех клетках, однако наиболее мощным генератором свободных радикалов служат лейкоциты и тромбоциты, а также гепатоциты [3].
Физиологическая роль свободных радикалов достаточно велика. Большая часть свободных радикалов генерируются фагоцитами, Т-лимфоцитами при воспалительных реакциях и выполняют защитную роль, лизируя патогенные микроорганизмы, мутировавшие (раковые) клетки. Свободнорадикальные процессы лежат в основе синтеза циклических и алифатических гидроперекисей, служащих интермедиаторами ферментативного синтеза простагландинов и лейкотриенов. Важнейшую физиологическую роль выполняет генерируемый в эндотелии сосудов оксид азота NO (эндотелий-зависимый релаксирующий фактор), обеспечивающий расслабление гладкой мускулатуры сосудистой стенки и регулирующий уровень артериального давления, коронарный и органный кровоток, а также предотвращающий агрегацию тромбоцитов.
Сами по себе свободные радикалы, перекиси крайне токсичны. Они окисляют фосфолипиды и белки клеточных мембран, нарушая их целостность, инактивируют клеточные и мембранные ферменты.
В противовес свободнорадикальным процессам в организме существует антиоксидантая система, представленная в первую очередь системой антиоксидантных ферментов: супероксиддимутазой (СОД), связывающей активные формы кислорода с образованием перекиси водорода; каталазой, деструктирующей перекиси в липидные гидропероксиды, глютатионпероксидазой (ГПО), редуцирующей липидные гидропероксиды за счет окисления глютатиона, глютатионредуктазой, восстанавливающей глютатион путем окисления НАДФН, последний восстанавливается через цитохромную цепь и систему природных антиоксидантов — α-токоферол, аскорбиновая кислота, флавоноиды.
Таким образом, про- и антиоксидантная системы находятся в состоянии динамического равновесия, что поддерживается определенной организацией плазменных и клеточных липидов, динамической системой обмена мембранных фосфолипидов и холестерина, определяющих исходный уровень жесткости и окисляемости клеточных мембран.
Чрезмерная активация свободнорадикальных процессов влечет за собой целый каскад негативных реакций и патологических процессов, лежащих в основе ряда заболеваний. Среди наиболее изученных на сегодняшний день свободнорадикальных патологий являются атеросклероз, ишемическая болезнь сердца, артериальная гипертония, в развитии которых большое значение приобретает неконтролируемая генерация пероксидов. Исходная активация свободнорадикальных процессов при атеросклерозе обусловлена снижением активности естественных антиоксидантных ферментов и дефицитом природных антиоксидантов, а также наличием дислипидемии, при которой содержащиеся в высокой концентрации в крови атерогенные липиды служат легким субстратом для перекисного окисления.
В последнее время, говоря о механизмах атерогенеза, многие авторы придают большое значение перекисной модификации липопротеидов низкой плотности (ЛНП) — липидно-белковых комплексов, обеспечивающих транспорт холестерина в эндотелиальные клетки. У модифицированных липопротеидов низкой плотности замедляется катаболизм, что становится причиной развития дислипидемии. Они приобретают способность быстрее связываться с эндотелиальными рецепторами и транспортировать в эндотелий больше холестерина. Накопление в эндотелиальных клетках перекисно модифицированных ЛП, в состав которых входит окисленный ХС, а также хемотаксическое действие тромбина и ряда других факторов свертывания, активированных липопероксидами, стимулируют миграцию в эндотелий из кровяного русла моноцитов и захват холестерина. Проникшие через межклеточные пространства макрофаги начинают интенсивно захватывать модифицированные ЛП, при этом модифицированные ЛП захватываются в десятки раз быстрее, чем обычные. Пересыщенные ХС макрофаги превращаются в пенистые клетки, подавляющая часть которых быстро погибает, в результате чего в интиму изливается накопленный ЭХС, НЭХС, кристаллы моногидрата ХС, формируется липидная инфильтрация артериальной стенки. Гибели пенистых клеток способствуют перекиси, нарушающие структурную целостность клеточной и плазматических мембран. Накопившиеся в интиме липопероксиды, ХС, тромбоцитарные и фибробластные факторы роста стимулируют миграцию гладкомышечных клеток из медии с последующей их пролиферацией, что в итоге приводит к формированию атеросклеротической бляшки. Доказательством главенствующей роли перекисно модифицированных ЛНП в развитии атеросклероза служит тот факт, что в экспериментальных работах на культуре клеток in vitro инактивация окисления ЛНП с помощью природных или синтетических антиоксидантов предотвращала миграцию макрофагов в интиму, задерживала формирование атеросклеротической бляшки. Применение антиоксидантов (пробукола) у кроликов линии Watanabe с гиперхолестеринемией также препятствовало развитию атеросклероза, при этом ПОЛ инактивировалось как в гепатоцитах, так и в интиме сосудов. У больных атеросклерозом применение антиоксиданта пробукола предотвращало развитие рестенозов после ангиопластики [3].
При стенокардии активация перекисных процессов обусловлена частыми ангинальными приступами, вызывающими гиперкатехоламинемию, стимулирующую липолиз, в результате которого увеличивается содержание свободных жирных кислот, являющихся доступным субстратом для окисления. При гипоксии (ишемии) миокарда окислительные процессы в митохондриях кардиомиоцитов нарушаются (как бы не доходят до конца), в результате чего накапливаются промежуточные метаболиты цикла Кребса, крайне легко подверженные восстановлению с образованием свободных радикалов и перекисных соединений, угнетающих систему антиоксидантной защиты. В конечном итоге создается парадоксальная ситуация — уменьшение кислорода в клетке приводит к увеличению кислородных радикалов. Развивающаяся после каждого эпизода транзиторной ишемии реперфузия миокарда также сопровождается значительной активацией (в сотни раз) свободнорадикальных процессов и выбросом липопероксидов в кровоток. Выраженная активация процессов свободнорадикального окисления и следующая за ним реакция тканей и систем организма получили название оксидативного стресса.
Велика роль свободнорадикального окисления (СРО) в патогенезе нестабильной стенокардии и инфаркта миокарда. Локальная активация СРО в зоне ишемии и накопление продуктов деградации свободных радикалов стимулируют свертываемость крови, увеличивают ее вязкость, усиливают агрегацию и адгезию форменных элементов крови. Высокая концентрация пероксидов ускоряет дегенерацию NO с образованием пероксинитрита — крайне цитотоксичного соединения: О2– +NOо ->ОNOO–. Ускоренный распад эндотелиального NO стимулирует ангиоспазм, а окисление экзогенного NO, образующегося в результате метаболизма потребляемых больным нитропрепаратов, уменьшает их терапевтическую эффективность. Кроме того, свободные радикалы модифицируют эндотелиальные NO-рецепторы, уменьшая их чувствительность, а также оказывают непосредственное повреждающее действие на кардиомиоциты. Указанные процессы усугубляют ишемию, оказывают аритмогенный эффект, способствуют распространению зоны некроза и повреждения.
Активация свободнорадикальных процессов при артериальной гипертензии ведет к уменьшению синтеза эндогенного NO, связывает NO при реакции липидными радикалами, тем самым снижает эндотелий-зависимую вазодилатацию, уменьшает эффективность многих классов гипотензивных препаратов, так как они реализуют свою фармакологическую активность через систему эндогенного NO.
Одна из популярных в настоящее время гипотез старения основана на положении о накоплении клеточных повреждений, вызванных воздействием свободных радикалов, что косвенно подтверждается угасанием активности антиоксидантной системы организма с возрастом.
Как показали клинико-экспериментальные исследования, проведенные за последние 10 лет в этой области, коррекция прооксидантных нарушений в проантиоксидантной системе при атеросклерозе, различных формах ишемической болезни сердца, артериальной гипертонии значительно улучшает клиническое течение нестабильной стенокардии, инфаркта миокарда, артериальной гипертензии, уменьшает прогрессирование атеросклероза.
Основной группой препаратов, способной противостоять оксидативному стрессу, являются антиоксидантные средства, инактивирующие свободные радикалы и препятствующие их образованию, участвующие в восстановлении антиоксидантов, или препараты, обладающие опосредованной антиоксидантной активностью. Последние непосредственно не являются антиоксидантами, но способны либо активировать антиоксидантную систему, либо повышать эффективность природных антиоксидантов, либо препятствовать окислению потенциальных субстратов.
Как указывалось выше, система антиоксидантной защиты имеет несколько «эшелонов обороны» и включает целый комплекс ферментативных систем и природных соединений, позволяющих утилизировать свободные радикалы, предотвратив их негативное воздействие на организм. Однако терапевтическое использование таких соединений на практике для лечения пациентов во многих случаях нереально либо по причине их нестойкости, либо из-за того, что они не усваиваются организмом. Кроме того, некоторые антиоксиданты идеально эффективны в биохимическом плане как утилизаторы пероксидов в экспериментах in vitro, но при парентеральном или пероральном применении вызывают серьезные побочные эффекты, исключающие их применение в клинической практике.
Недостаточная популярность антиоксидантных средств и отсутствие традиций их широкого применения в практической медицине обусловлены рядом причин: недостаточной изученностью этого вопроса, сложностью адекватной оценки состояния параметров перекисного окисления в организме, отсутствием эффективных медикаментозных средств, обладающих антиоксидантной активностью и способных быстро уменьшить последствия оксидативного стресса.
К сожалению, в настоящее время не существует общепринятой классификации антиоксидантных препаратов. Как правило, антиоксиданты разделяют на природные и синтетические. К природным антиоксидантам относятся α-токоферол (витамин Е), β-каротин. Их применение уменьшает риск развития и прогрессирования атеросклероза, несколько снижает высокий уровень липопероксидов в крови больных хроническими формами ИБС, артериальной гипертонии. Однако для достижения эффекта их применение должно быть достаточно долгим (месяцы), в связи с чем указанные средства представляют интерес только в качестве профилактических препаратов.
Определенными антиоксидантными свойствами обладает аскорбиновая кислота. Она способна восстанавливать окисленные α-токоферольные радикалы, возвращая α-токоферолу его антиоксидантные свойства, а также непосредственно связывать супероксидионы и активные радикалы. Однако ее антиоксидантная активность невелика и проявляется лишь в малых концентрациях. В высоких концентрациях она выступает как прооксидант. Указанные свойства аскорбиновой кислоты позволяют использовать ее преимущественно как профилактическое средство.
В последние годы довольно активно стали использоваться в качестве пищевых добавок или в составе витаминных комплексов ионы металлов с переменной валентностью (селен, марганец, медь, цинк), которые входят в состав активных центров ряда природных антиоксидантных ферментов (супероксиддисмутаз) и потому способны существенно увеличивать их активность. Особую значимость использование таких препаратов приобретает в географических зонах с низким содержанием указанных элементов в воде и пище.
К другим природным антиоксидантным соединениям относятся флавоноиды, в большом количестве содержащиеся в виноградных косточках, ягодах черники, листьях гинкго билобы, сухом красном вине. Флавоноиды тормозят свободнорадикальные процессы на уровне инициации, взаимодействуя с активными радикалами. Однако в настоящее время доказана их эффективность только in vitro, убедительных данных о доминирующей антиоксидантной активности флавоноидов in vivo пока не получено.
Определенную антиоксидантную активность имеют SH-содержащие аминокислоты (цистеин, цистин, метионин), при этом SH-группы выступают как конкурирующие с другими субстратами объекты окисления, не дающие свободных радикалов и фактически гасящие цепную реакцию свободнорадикального окисления. SH-содержащие соединения способны пролонгировать продолжительность «жизни» молекулы NO. Однако терапевтическое применение соединений, содержащих SH-группы (глютатион, тиоловая кислота, N-ацетилцистеин), ограничивается из-за невысокой их проницаемости через цитоплазматические мембраны, где они могут являться защитниками от внутриклеточного оксидативного стресса, а также из-за способности активировать перекисные реакции во внеклеточной среде.
Умеренной антиоксидантной активностью обладают женские половые гормоны (эстрадиол, эстрагон, эстриол), чем, вероятно, обусловлена нераспространенность атеросклероза у женщин в детородном возрасте. Описана опосредованная антиоксидантная активность у мелатонина. Однако клиническое использование гормональных средств в качестве антиоксидантов представляется весьма проблематичным.
В последние годы предпринимаются небезуспешные попытки клинического использования коэнзима Q (убихинона) — одного из самых распространенных соединений в клетках бактерий и животных, сходного по химической структуре с α-токоферолом. Однако возможности, которыми обладает коэнзим Q, и целесообразность его применения служат в настоящее время предметом изучения.
Большой интерес представляют в клиническом плане синтетические антиоксиданты или препараты, обладающие антиоксидантной активностью. Наибольшей эффективностью, отсутствием токсичности и минимальными побочными эффектами характеризуются производные 3-оксипиридина — эмоксипин, мексикор. Эмоксипин является, пожалуй, одним из первых синтетических антиоксидантных средств, вошедших в широкую клиническую практику. Опыт применения раствора эмоксипина у больных с острым инфарктом миокарда на фоне традиционной терапии показал, что препарат существенно улучшал клиническое течение болезни, снижал частоту фатальных осложнений, увеличивал выживаемость больных в острый и подострый период инфаркта.
Мексикор, сходный с эмоксипином по механизмам действия, обладает значительно большей антиоксидантной активностью, выпускается в разрешенной к клиническому применению капсулированной (для перорального приема) и водорастворимой инъекционной форме для парентерального введения. Это позволяет использовать препарат в любых фазах инфаркта и при нестабильной стенокардии, а также сохранить преемственность терапии, переходя с инъекционных форм (на острой стадии болезни) на капсулированную форму (в последующий подострый период или период стабилизации).
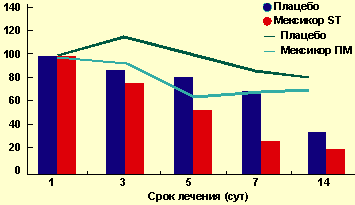
Рандомизированное плацебо-контролируемое исследование мексикора у больных с нестабильной стенокардией показало, что пероральное применение препарата в дозе 6 мг/кг/сут на фоне комплексной традиционной терапии антикоагулянтами, антиагрегантами и антиангинальными средствами, в сравнении с контрольной группой, значительно ускоряло стабилизацию стенокардии, снижало частоту и продолжительность периодов ишемии, а также суммарный интеграл суточного смещения сегмента ST (рисунок 1) и, кроме того, сокращало частоту желудочковых нарушений ритма по результатам холтеровского мониторирования. Указанные изменения сопровождались быстрой нормализацией концентрации продуктов перекисного окисления липидов в крови.
| Рисунок 1. Изменения интеграла смещения ST и отношения болевых/безболевых периодов ишемии у больных нестабильной стенокардией на фоне терапии мексикором. |
 |
Как показали экспериментальные исследования на изолированных сегментах артерий собак, мексикор существенно усиливал вазодилатирующие эффекты нитроглицерина, а при экспериментальной модели окклюзионного инфаркта миокарда у собак повышал объемную скорость коронарного кровотока, сохраняя положительное действие на его фазовую структуру.
Клинические исследования подтверждают способность мексикора увеличивать антиангинальную эффективность пролонгированных нитратов у больных стабильной стенокардией II—III функционального класса: применение мексикора в дозе 0,3-0,4 г/сут. в течение двух месяцев на фоне неизменной дозы пролонгированных нитратов позволило повысить пороговую мощность при велоэргометрическом тесте через один месяц (рисунок 2).
| Рисунок 2. Изменения величины пороговой мощности ВЭМ на фоне терапии мексикором и нитратами больных стабильной стенокардией. |
 |
Открытое рандомизированное исследование инъекционной формы мексикора (6 мг/кг/сут в течение двух недель с последующим переходом на капсулированную форму до одного месяца) у больных острым инфарктом миокарда показало, что мексикор существенно ускорял, в сравнении с контролем, восстановление диастолической функции левого желудочка (оценка производилась по параметрам трансмитрального потока). Мексикор улучшал сегментарную сократимость левого желудочка, ускоряя переход отдельных сегментов миокарда левого желудочка в периинфарктной зоне из состояния акинеза в гипокинез, гипокинеза — в нормокинез (рисунок 3).
| Рисунок 3. Число зон акинезии у больных острым инфарктом на фоне терапии мексикором. |
 |
Клиническое использование мексикора в комплексной терапии артериальной гипертонии с кризовым течением позволяет сократить сроки стабилизации давления, уменьшить частоту рецидивирования кризов на постгоспитальном этапе, повысить эффективность гипотензивной терапии.
Преимущество мексикора как средства выбора при лечении острой сердечно-сосудистой патологии, наряду с высокой эффективностью, обусловлено наличием парентеральной формы препарата, применение которой позволяет быстро создать терапевтическую концентрацию и получить клинический эффект.
Определенной опосредованной антиоксидантной активностью обладают некоторые гипохолестеринемические препараты — статины (симвастатин), противоишемический препарат триметазидин, некоторые ингибиторы АПФ, а также β-адреноблокаторы. Механизм действия последних обусловлен ограничением катехоламинемии, снижением интенсивности липолиза и уменьшением содержания в крови легко окисляемых свободных жирных кислот. Однако позитивные антиоксидантные эффекты указанных средств, хотя и позволяют отдать им предпочтение при выборе лекарств у больных с атеросклерозом и артериальной гипертонией, все же являются второстепенными, что следует учитывать при назначении этих лекарственных средств по основным показаниям.
Пробукол долгое время считался перспективным антиоксидантным препаратом, однако отсутствие инъекционной формы, позднее развитие антиоксидантного эффекта (месяцы), наличие осложнений (удлинение интервала QT) не позволили использовать этот препарат достаточно широко.
Следует также помнить, что позитивная фармакодинамика кардиопротективных и противоишемических лекарственных средств (триметазидин, милдронат) лишь в некоторой степени связана с подавлением в ишемизированных тканях свободнорадикальных процессов, все-таки основной точкой приложения этих препаратов является оптимизация клеточного энергетического обмена, уменьшение потребности ишемизированной ткани в кислороде.
Таким образом, имеющийся на сегодняшний день клинический опыт и результаты экспериментальных исследований свидетельствуют о важной роли оксидативного стресса в формировании и прогрессировании сердечно-сосудистой патологии и необходимости его ранней, планомерной и комплексной антиоксидантной коррекции.
Литература
- Владимиров Ю. А., Арчаков А. И. Перекисное окисление липидов в биологических мембранах. - М.: Наука,1972. - 256 с.
- Зенков Н. К., Ланкин В. З., Меньшикова Е. Б. Окислительный стресс. - М.: Наука, 2001. - 342 с.
- Ланкин В. З., Тихазе А. К., Беленков Ю. Н. Свободнорадикальные процессы в норме и при патологических состояниях. - М., 2001. - 78 с.
А. П. Голиков, доктор медицинских наук, профессор, академик РАМН
С. А. Бойцов, доктор медицинских наук, профессор
В. П. Михин, доктор медицинских наук, профессор
В. Ю. Полумисков, кандидат медицинских наук, доцент
НИИ СП им. Н. В. Склифосовского, Государственный медицинский центр, Медицинский центр УД Президента РФ (Москва), Курский ГМУ
.jpg)
.jpg)
.jpg)









