Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) — безусловный лидер среди кислотозависимых заболеваний. Проведенными эпидемиологическими исследованиями установлена высокая распространенность в различных регионах России типичных, классических, проявлений ГЭРБ, прежде всего изжоги и кислотной регургитации [1]. В экономическом аспекте наличие изжоги у работающего пациента означает сокращение продолжительности его рабочего времени и уменьшение производительности труда, зависимых от выраженности и персистирования симптомов. Проблема своевременной диагностики ГЭРБ гораздо шире, чем только адекватная оценка ее классических эзофагеальных проявлений.
Так, при наблюдении за более чем 8,5 тысячами больных ГЭРБ за 20-летний период риск развития ларингита оказался в 5,9 раз выше, чем среди прочего населения, бронхита и астмы — в 2 раза, пневмонии — в 1,4 раза. Безусловно, поздняя диагностика ГЭРБ с экстраэзофагеальными проявлениями неизбежно приводит к необоснованному применению лекарственных средств с увеличением прямых и непрямых затрат на лечение, снижению трудоспособности, развитию синдрома лекарственного отягощения и, в конечном итоге, сопровождается увеличением общественных потерь [2].
Современные диагностические и терапевтические подходы к курации пациентов с ГЭРБ определены международными консенсусами (Генвальским 1999 года [3] и Монреальским 2006 года [4]), которыми определена неоднородность популяции как в зависимости от наличия или отсутствия эрозий слизистой оболочки пищевода, так и в зависимости от наличия или отсутствия экстраэзофагеальных проявлений заболевания. Особенностью заболевания является отсутствие клинических маркеров повреждения слизистой оболочки пищевода с формированием эрозий [5], а также наличием структурных изменений слизистой оболочки у пациентов с неэрозивной формой рефлюксной болезни (НЭРБ) при морфологическом исследовании [6].
Вне зависимости от формы ГЭРБ следует стремиться к достижению следующих «конечных точек» или целей терапии больного:
-
максимально быстрое купирование клинических симптомов;
-
эпителизация эрозий слизистой оболочки пищевода при их наличии;
-
предотвращение рецидивов и осложнений;
-
повышение качества жизни.
Терапевтическая стратегия курации пациента с диагностированной ГЭРБ включает модификацию питания и образа жизни [7], а также назначение лекарственных средств.
Модификация питания и образа жизни предполагает выполнение пациентом следующих рекомендаций:
-
после принятия пищи избегать наклонов вперед и не ложиться спать с приподнятой головой;
-
не носить тесную одежду и тугие пояса;
-
избегать обильных приемов пищи;
-
не есть на ночь;
-
ограничить потребление продуктов, вызывающих снижение давления нижнего пищевого сфинктера (НПС) и оказывающих раздражающее воздействие (жиры, алкоголь, кофе, шоколад, цитрусовые);
-
отказаться от курения;
-
нормализовать вес.
Соблюдение этих рекомендаций необходимо не только для уменьшения выраженности проявлений заболевания, но и для снижения трансформации текущей формы ГЭРБ в более тяжелую, например, неэрозивной формы в эрозивную. К значимым неблагоприятным прогностическим факторам по трансформации в эрозивную форму относятся: курение (OR 3,1), ожирение (OR 3,5). Вместе с тем прием ингибиторов протонной помпы (ИПП), напротив, снижает риск прогрессирования более чем в три раза [8].
Помимо модификации характера питания и образа жизни, лечебные мероприятия включают и медикаментозную терапию заболевания: антациды/алгинаты, блокаторы Н2-рецепторов гистамина и ИПП, а также средства, нормализующие моторику (прокинетики).
Прокинетики, регулируя моторную функцию прежде всего верхних отделов пищеварительного тракта, относятся к средствам патогенетической терапии. Эта группа средств включает метоклопрамид, домперидон и итоприд.
Метоклопрамид усиливает высвобождение ацетилхолина в желудочно-кишечном тракте (стимулирует моторику желудка, тонкой кишки и пищевода), блокирует центральные дофаминовые рецепторы (воздействие на рвотный центр и центр регулирования желудочно-кишечной моторики). Метоклопрамид повышает тонус НПС, ускоряет эвакуацию из желудка, оказывает положительное влияние на пищеводный клиренс и уменьшает гастроэзофагеальный рефлюкс. К недостаткам метоклопрамида следует отнести его нежелательное центральное действие (головная боль, бессонница, слабость, импотенция, гинекомастия, усиление экстрапирамидальных расстройств).
Эффективность периферического блокатора рецепторов дофамина (домперидон) как прокинетического агента не превышает таковую метоклопрамида, но препарат не проходит через гематоэнцефалический барьер и практически не оказывает побочных действий.
Итоприд (Ганатон) является одновременно антагонистом допаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации, обладает минимальной способностью проникать через гематоэнцефалический барьер в центральную нервную систему, включая головной и спинной мозг. Метаболизм препарата позволяет избежать нежелательного лекарственного взаимодействия при приеме лекарственных препаратов, метаболизирующихся ферментами системы цитохрома Р450. Как показали экспериментальные и клинические исследования, итоприд усиливает пропульсивную моторику желудка и ускоряет его опорожнение. Кроме того, препарат оказывает противорвотный эффект, которой реализуется благодаря взаимодействию с D2-дофаминовыми хеморецепторами триггерной зоны.
Применение прокинетиков патогенетически обосновано, однако эффективность монотерапии прокинетиками уступает терапии ИПП, в связи с этим препараты, нормализующие моторную активность пищеварительного тракта, применяются как средства сопровождения к ИПП.
Антациды (от греч. anti — против, лат. acidus — кислый) — группа лекарственных препаратов, снижающих кислотность содержимого желудка за счет химического взаимодействия с соляной кислотой желудочного сока. Антацидные препараты классифицируют по действующему началу, основному составному компоненту (магний-, алюминий-, кальцийсодержащие и др.), по заряду активного иона (анионные и катионные), по степени всасывания в кишечнике. К всасывающимся компонентам антацидных препаратов относятся натрия гидрокарбонат (сода), кальция карбонат основной, магния оксид (жженая магнезия), магния карбонат основной и некоторые другие. На их основе издавна составлялись кислотонейтрализующие смеси, такие как смесь Бурже (натрия бикарбонат, натрия сульфат, натрия фосфат), смесь Ренни (кальция карбонат основной, магния карбонат основной), смесь Тамс (кальция карбонат, магния карбонат). Интенсивно нейтрализуя соляную кислоту, эти средства имеют непродолжительное по времени действие с последующим эффектом «рикошета» — повторным усилением желудочной секреции. Нейтрализация кислоты сопровождается образованием углекислого газа, который может провоцировать гастроэзофагеальный рефлюкс, что ограничивает сферу применения этих препаратов.
Более того, растяжение желудка, вызываемое углекислым газом, стимулирует усиление желудочной секреции. Этому же способствует слишком быстрое ощелачивание среды в желудке с активизацией кислой секреции по принципу отрицательной обратной связи. Наконец, всасывание бикарбонатов в кровь в высоких дозах может привести к развитию системного алкалоза. В связи с этим на сегодняшний день предпочтение отдается невсасывающимся антацидам, которые хотя и медленнее нейтрализуют соляную кислоту, но не вызывают эффекта «рикошета» и не оказывают системных эффектов. К ним относятся алюминия гидроксид, алюминия фосфат, магния гидроксид, магния трисиликат. Невсасывающиеся антациды обладают высокой безопасностью, но и они могут вызывать некоторые побочные эффекты. Так, препараты алюминия способствуют замедлению моторики кишечника, а магния — ускорению. Поэтому в современных антацидных препаратах часто используется сбалансированная комбинация солей магния и алюминия. Например, препарат Гастал состоит из высушенного геля гидроталцита (450 мг в 1 таблетке) и гидроксида магния (300 мг 1 в таблетке). Таблетированная форма Гастала препарата удобна своей универсальностью: она может быть использована и для регулярного приема в течение курсового лечения, и для разового применения «по требованию». Гастал выпускается в виде таблеток для рассасывания, которые не требуют запивания водой, что очень удобно.
Для Гастала характерно не только их высокая кислотонейтрализующая активность, но также способность адсорбировать желчные кислоты, лизолецитин и пепсин, высокие буферные свойства, быстрое начало и значительная продолжительность действия, хорошие органолептические свойства при минимальной возможности каких-либо побочных эффектов. Кроме того, Гастал обладает цитопротективным эффектом, а также стимулирует процессы клеточной регенерации.
К антацидным средствам примыкают и алгинаты (от лат. alga — морская трава, водоросль, представитель группы — Гевискон), образующие невсасывающийся алгинатный гелевый барьер на поверхности содержимого желудка. Если рефлюкс происходит, то алгинатный гель первым проникает в пищевод и оказывает протективное действие.
Монотерапия антацидами/алгинатами, к сожалению, не может обеспечить достижения всех целей терапии ГЭРБ и лимитирована только периодом беременности. Вместе с тем антациды и алгинаты должны быть рекомендованы больным в режиме «по требованию», а также (при необходимости) в качестве компонента комплексной курсовой терапии в сочетании с ИПП и прокинетиками.
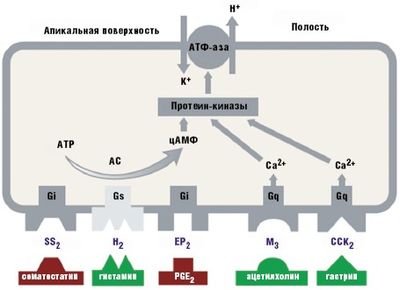
ИПП и блокаторы Н2-рецепторов гистамина. ИПП сегодня относятся к препаратам выбора для пациентов, страдающих ГЭРБ. Этот класс препаратов ингибирует конечный этап транспорта протонов — Н+/К+-АТФазы (рис.) вне зависимости от того, взаимодействием с каким рецептором была активирована протонная помпа. Сегодня фармацевтический рынок предлагает несколько препаратов этой группы (омепразол, эзомепразол, лансопразол, пантопразол, рабепразол), одинаковых по механизму своего действия (блокада протонного насоса), но, тем не менее, различных в быстроте, глубине действия и продолжительности кислотной супрессии, что обусловлено разной молекулярной структурой и особенностями фармакокинетики и фармакодинамики.
Результаты метаанализа работ, посвященных сравнительной оценке эффективности использования блокаторов желудочной секреции, показали, что частота заживления эрозий слизистой оболочки пищевода в течение 12 недель лечения составляет при применении ИПП более 80%, а при использовании блокаторов Н2-рецепторов гистамина — менее 50% [9]. Эти данные полностью подтверждают правило Белла (1992), в соответствии с которым эрозии пищевода заживают в 80–90% случаев при условии поддержания в пищеводе рН > 4 не менее 16–22 часов в течение суток [10], что достигается только при использовании ИПП. В связи с этим ИПП в настоящее время признаны наиболее эффективными средствами для лечения ГЭРБ и должны назначаться при всех ее стадиях [11]. Продолжительность лечения зависит от выбранного варианта терапии и ее эффективности и может колебаться в среднем от 4 до 26 недель.
Эффективность ИПП превышает как эффективность плацебо, так и Н2-гистаминоблокаторов и прокинетиков и в профилактике осложнений и рецидивов заболевания. Прием ИПП ассоциирован со снижением частоты формирования дис/неоплазии, ассоциированной с пищеводом Барретта [12], а также со снижением частоты формирования аденокарциномы, ассоциированной с пищеводом Барретта [13].
В опубликованном в 2009 году консенсусе по диагностике и лечению НЭРБ [14] международными экспертами отмечено, что редукция симптомов под влиянием стандартной терапии хуже, чем при эрозивной форме заболевания. При персистенции симптомов у больного НЭРБ необходим двукратный прием препарата, а при неполном контроле симптомов следует дополнить лечение антацидами/алгинатами.
Клинический опыт показывает, что, несмотря на назначение ИПП дважды в день, у 10–30% пациентов симптомы ГЭРБ могут частично или полностью сохраняться. Таких пациентов с эрозивной или неэрозивной формами ГЭРБ называют «не отвечающими на терапию ИПП» (PPI non-responders), т. е. рефрактерными к проводимой терапии. В последних согласительных документах указывается, что о резистентной к ИПП НЭРБ можно говорить лишь по истечении 12 недель. С чем связана эта рефрактерность и как вести таких пациентов? Во-первых, необходимо убедиться, что рекомендованные препараты пациентом принимаются правильно, без пропусков, с необходимой кратностью и в необходимой дозе. Известно, что эффективность ИПП может определяться особенностями метаболизма этих средств, а также снижением биодоступности, что требует в таких случаях назначения наиболее эффективных ИПП с минимальным риском лекарственного взаимодействия и предсказуемой скоростью метаболизма (рабепразол, эзомепразол).
Затем следует убедиться в том, что имеется кислый, а не щелочной рефлюкс, обусловленный сопутствующим дуоденогастральным рефлюксом, с присутствием в рефлюктате желчных кислот, поскольку в таком случае потребуется включение в комплекс терапии антацидов и прокинетиков [15]. Наконец, следует пересмотреть диагноз с исключением других заболеваний со сходной симптоматикой (например, функциональная изжога, эозинофильный эзофагит).
Таким образом, залог успешной терапии больного — это своевременно установленный диагноз, приверженность пациента к выполнению рекомендаций по модификации питания, образа жизни, а также терапия с включением эффективных и максимально безопасных средств в адекватных дозах и необходимой продолжительности.
Литература
-
Маев И. В., Кучерявый Ю. А. Достижения в диагностике и лечении гастроэзофагеальной рефлюксной болезни // Фарматека. 2007, № 2. С. 49–52.
-
Gisbert Javier P., Cooper A., Karagiannis D. et al. Impact of gastroesophageal reflux disease on work absenteeism, presenteeism and productivity in daily life: a European observational study Published: 16 October 2009 Health and Quality of Life Outcomes 2009, 7:90 doi:10.1186/1477–7525–7-90.
-
Dent J., Brun J., Fendrick A. M. et al. An evidence-based appraisal of reflux disease management: the Genval Workshop Report // Gut 1999; 44 (suppl 2): S1–S16.
-
Vakil N., van Zanten S. V., Kahrilas P., Dent J., Jones R. and the Global Consensus Group. Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus // Am. J. Gastroenterol. 2006. V. 101. P. 1900–1920.
-
Martinek J., Benes M., Hucl T., Drastich P., Stirand P., Spicak J. Non-erosive and erosive gastroesophageal reflux diseases: no difference with regard to reflux pattern and motility abnormalities // Scand J Gastroenterol. 2008; 43: 794–800.
-
Kiesslich R., Kanzler S., Vieth M., Moehler M., Neidig J., Thanka Nadar B. J., Schilling D., Burg J., Nafe B., Neurath M. F., Galle P. R. Minimal change esophagitis: prospective comparison of endoscopic and histological markers between patients with non-erosive reflux disease and normal controls using magnifying endoscopy // Dig Dis. 2004; 22: 221–227.
-
Festi D., Scaioli E., Baldi F., Vestito A., Pasqui F., Di Biase A. R., Colecchia A. Body weight, lifestyle, dietary habits and gastroesophageal reflux disease // World J Gastroenterol. 2009; 15 (14): 1690–1701.
-
Pace F., Pallotta S., Manes G., de Leone A., Zentilin P., Russo L., Savarino V., Neri M., Grossi E., Cuomo R. Outcome of nonerosive gastro-esophageal reflux disease patients with pathological acid exposure // World J Gastroenterol. 2009; 15 (45): 5700–5705.
-
Holtmann G. The clinical usefulness of PPIs: Are they all the some? (Yes). «PPIs: Are they all the some? The Ultimate Debate». 10 UEGW, Absrtact Book. Geneva. 2002: 10–11.
-
Bell N. J. V., Burget D., Howden C. W. et al. Appropriate acid suppression for the management of gastro-esophageal reflux disease // Digestion. 1992; 51 (Suppl. 1): 59–67.
-
Donnellan C., Sharma N., Preston C., Moayyedi P. Medical treatments for the maintenance therapy of reflux oesophagitis and endoscopic negative reflux disease. Cochrane Database Syst Rev 2005: CD003245.
-
El-Serag H. B., Aguirre T. V., Davis S., Kuebeler M. Proton pump inhibitors are associated with reduced incidence of dysplasia in Barrett’s esophagus // Am J Gastroenterol. 2004; 99: 1877–1883.
-
Cooper B. T., Chapman W., Neumann C. S., Gearty J. C. Continuous treatment of Barrett’s oesophagus patients with proton pump inhibitors up to 13 years: observations on regression and cancer incidence // Aliment Pharmacol Ther. 2006; 23: 727–733.
-
Modlin I. M., Hunt R. H., Malfertheiner P. et al. Vevey NERD Consensus Group Diagnosis and Management of Non-Erosive Reflux Disease — The Vevey NERD Consensus Group Digestion. 2009; 80: 74–88.
-
Monaco L., Brillantino A., Torelli F., Schettino M., Izzo G., Cosenza A., Di Martino N. Prevalence of bile reflux in gastroesophageal reflux disease patients not responsive to proton pump inhibitors // World J Gastroenterol. 2009; 15 (3): 334–338.
М. А. Ливзан, доктор медицинских наук, профессор
Е. Е. Душеба
В. В. Юргель
ГОУ ВПО «Омская государственная медицинская академия Росздрава», Омск
Контактная информация об авторах для переписки: mlivzan@yandex.ru
Купить номер с этой статьей в pdf









